Tag: 癌症
研究人員發現膽固醇助長癌細胞轉移的其中一種方式
據媒體報導,由杜克大學癌症研究所領導的一項新研究發現了膽固醇可以增強癌細胞轉移的能力的方式之一。該研究特別關注乳腺癌,闡明了先前的觀察性研究將使用他汀類藥物與更好的存活率聯系起來。 ...
縮小啤酒肚的對策,終於來了
肥胖會引起一系列健康問題,而問題最大的肥胖類型要數內髒脂肪過度積累引起的肥胖,外觀的表現就是腹部的「游泳圈」、「啤酒肚」。腹腔深處,脂肪包圍著重要的器官,為各種基本功能提供支持;但是如果內髒脂肪過於豐富,對鄰近組織和器官就會產生慢性炎症等負面影響。 過量的內髒脂肪非常危險,而且還很難消除。一些研究發現,即便管住嘴刻意少吃,也很難有效減少腹部脂肪。
葡萄牙Champalimaud研究與診斷中心的科研小組決定著手探索「自然燃脂」的機制,希望從中找出潛在的臨床應用。最近,他們的研究成果登上了頂尖學術期刊《自然》。在這篇論文中,研究人員首次揭示了神經系統和免疫系統通過相互作用指導內髒脂肪存儲的過程。這一發現為對抗肥胖和肥胖相關疾病提供了多種新的對策。
很多人或許以為內髒脂肪就是均勻的一大坨油脂,實際上里面除了脂肪細胞,還含有神經纖維和多種類型的細胞,包括免疫細胞。
其中一種叫ILC2(2型天然淋巴細胞)的免疫細胞引起了這支研究小組的注意。「ILC2在很多組織和器官里對各種免疫功能至關重要,包括維持脂肪組織的健康狀態。」研究一作Ana Filipa Cardoso博士介紹。
他們發現,內髒脂肪中,神經末梢與ILC2之間的交流需要一個關鍵的「中介」:間充質細胞(mesenchymal cell)。
這一發現出人意料,因為很長時間以來,間充質細胞只被看作是組織中的「腳手架」。研究負責人Henrique Veiga-Fernandes教授說:「間充質細胞一直以來被廣泛忽視,直到最近十多年,科學家們才發現,間充質細胞發揮多種重要的積極作用。」
一系列實驗指出,脂肪組織中的間充質細胞就像翻譯,接收到交感神經末梢發送的信號後,向ILC2發送信息,然後由ILC2命令脂肪細胞增強脂質代謝、消耗能量,避免過量脂肪引起胰島素抵抗和肥胖的傾向。研究人員指出,間充質細胞在內髒脂肪組織中扮演的角色,非常適合用來精準調節其他細胞的活動。
在確認了內髒脂肪的這一燃脂機制後,研究小組繼續追溯源頭,尋找交感神經末梢的信號是從哪里來的。「內髒脂肪中的神經纖維屬於外周神經系統,但它們不是『老闆』,它們受到大腦所屬的中樞神經系統的指揮。」 Cardoso博士解釋。
利用逆行示蹤技術和外科手術、化學遺傳學等操作,最終研究人員確認,下丘腦室旁核(PVH)位於這條神經環路的上級指揮中心。下丘腦在大腦底部,是一系列重要過程的控制中心,包括新陳代謝、生殖、胃腸道和心血管功能。
「這一發現意義重大。」Veiga-Fernandes教授說,「我們第一次發現這樣的神經環路,這條長距離的神經環路將大腦信息轉化為與肥胖有關的免疫功能。」
這一發現進一步引出了許多新的問題,例如,是什麼觸發下丘腦室旁核發出「燃脂」的指令,與特定的飲食或鍛鍊有關嗎?還是依賴內部的代謝信號?找出這些問題的答案,對於預防和治療肥胖具有指導意義。
研究小組表示,在他們揭示的長距離、多步驟過程中,有多個可能的切入點,有望調節內髒脂肪燃燒,對抗肥胖並降低心血管疾病、癌症等與肥胖有關的疾病的風險。
據Veiga-Fernandes教授期待,目前研究機構下屬的初創公司LiMM正在計劃靶向神經免疫過程,轉化為創新的治療方法。期待研究人員的發現早日帶來臨床應用。
來源:cnBeta
磁場消滅癌細胞 是一種新的抗癌方案嗎?
最影響人類生命質量的疾病排在首位的就是癌症了。古人談虎色變,今人談癌色變。癌症這類疾病早已經不是年老體弱的人專屬,而是越來越趨於年輕化。有多少人每年體檢完,最不敢面對的就是體檢單,賈玲在春晚的小品中也曾調侃:小病不用治,大病治不了,去體檢,反而耽誤事情。 ...
研究顯示增加維生素D攝入量可預防年輕時患結直腸癌
根據一項研究顯示,攝取來自飲食的較多維生素D,可能有助於防止患上年輕發病的結腸癌或結腸癌前息肉。這項研究最近在線發表在《胃腸病學》雜誌上,它由來自丹娜法伯癌症研究所、哈佛大學陳氏公共衛生學院和其他機構的科學家進行。這項研究有可能導致建議增加維生素D的攝入量,作為篩查測試的廉價補充,並且作為50歲以下成年人的大腸癌預防策略。 ...
70%小鼠消除胰腺癌:華人科學家提出攻克癌症之王新方法
常被稱為「癌症之王」的胰腺導管腺癌(pancreatic ductal adenocarcinoma,PDAC),是胰腺癌中最常見的類型,也是各類實體瘤中最為凶險的癌症之一。在其他很多癌症中取得良好效果的化療、免疫療法等,遇到胰腺導管腺癌往往無力回天。 目前轉移性胰腺癌的標準治療為化療組合,客觀緩解率只有23%左右。一些臨床試驗顯示,在化療基礎上添加免疫療法,如PD-1抑制劑,也沒有提供額外獲益。
然而,日前頂尖學術期刊《細胞》上發表了一項令人振奮的研究,有望改變胰腺癌治療困難的局面。
領銜這項研究的是哈佛醫學院華人科學家盧坤平教授和周小珍教授。兩位科學家在過去多年的合作中,圍繞一種獨特的脯氨酸異構酶Pin1進行了詳細研究。這種酶通過影響其他蛋白的結構和磷酸化,調節很多與細胞周期有關的重要蛋白,其信號傳導的失調對多種癌症以及阿爾茨海默病的發展產生影響。
此次研究中,這支團隊發現,Pin1在胰腺導管腺癌患者的癌細胞和癌症相關成纖維細胞中都有過量表達,並且Pin1高表達與患者的不良生存率相關。因此,研究人員探索了靶向抑制Pin1治療胰腺癌的可能性。
實驗結果顯示,在多種胰腺癌模型小鼠中,使用臨床上已開發的Pin1抑制劑,與免疫療法PD-1抑制劑、化療藥物吉西他濱(gemcitabine)協同作用,可以完全消除或持續緩解小鼠體內的腫瘤!
在引入兩種致癌基因Kras和p53突變的胰腺癌小鼠中,如果僅用吉西他濱和PD-1抑制劑治療,效果甚微,大部分小鼠在3個月內死亡;然而,加入Pin1抑制劑的治療顯著提高了生存率,70%的小鼠在治療後至少存活6個月,並且體內的腫瘤消失了。
對於Pin1抑制劑為何能顯著增強免疫化療的效果,研究小組也對背後的機制進行了分析。他們發現,靶向Pin1可以同時阻斷多條癌症信號通路,並且通過作用於癌症相關成纖維細胞,解除腫瘤微環境的免疫抑制性;此外,靶向Pin1還可以誘導癌細胞多表達PD-1配體PD-L1,以及細胞攝取吉西他濱的轉運蛋白ENT1,讓癌細胞更容易被PD-1抑制劑和吉西他濱徹底鏟除。
我們期待這一潛在治療策略可以在後續的臨床試驗中取得順利結果,早日造福胰腺癌患者。
來源:cnBeta
我科學家取得重大科研成果 有望將肺癌變成慢性病
8月12日深夜,國際知名學術期刊《細胞·癌症》,刊發了廣東省肺癌研究所名譽所長吳一龍團隊的最新研究成果,即用於中國EGFR突變晚期非小細胞肺癌患者一線治療的新型聯合治療方法。該方法可延長患者的無進展生存期至17.9個月,意味著疾病進展風險降低了45%。 ...
微小的觸角顆粒可以偽裝植入物以避免免疫排斥反應
我們的免疫系統是保護我們安全的強大盟友,但有時它也會有點得寸進尺,攻擊那些試圖幫助我們的外來物甚至自身。現在,研究人員已經開發出了被稱為樹枝狀物的顆粒,這些顆粒覆蓋著微小的觸角,由於其實在太小,免疫系統無法檢測,可以方便地用於輸送藥物或偽裝植入物以防止排斥反應。 ...
科學家嘗試利用鈾的力量來治療癌症等疾病
科學家們已經開發出一種新的系統,用於生產「放射性同位素」,以治療癌症。該系統使用一個簡單的放射性核素發生器來重復分離釷-226和其壽命更長的母體同位素鈾-230。這兩種同位素都會發射放射性α粒子。這使它們成為用於靶向α治療劑的候選者。這些是傳遞目標粒子以治療疾病的物質。鈾-230/釷-226這對同位素具有獨特的優勢,在衰變時發射多個α粒子。這意味著它們可以向癌細胞提供更具破壞性的能量。
放射性同位素正日益成為治療醫學的關鍵工具。如果研究人員能夠獲得更多的放射性同位素,他們就能提高開發治療各種癌症的可能性。迄今為止,治療方法主要依靠β發射同位素來摧毀惡性細胞。由α發射同位素發出的α粒子對細胞的破壞力要遠遠大於β粒子。此外,α粒子在體內的射程很短,因此它們對周圍健康組織的損害要小得多。這也意味著α發射器可以有效地治療已經擴散或轉移的癌症。
近年來,研究人員已經開發了幾種用於"靶向α治療"的α發射器。這些包括鐳-223/224,錒-225和鉍-213。鈾-230/釷-226這一對具有獨特的優勢,在其衰變鏈中發射四個α粒子。這意味著它可以向病變細胞提供更多的破壞性能量。此外,鈾-230的生產不需要高能加速器,這意味著它最終可以在多種地點生產,以增加可用性。釷-226發生器很容易設置,商業供應商也很容易在研究和醫療設施中進行部署。
自從瑪麗和皮埃爾·居里發現鐳,以及隨後研究人員觀察到它可以縮小腫瘤以來,研究人員一直在尋求更多的放射性同位素用於診斷和治療。各個同位素不同的化學和衰變特性使每個同位素都獨特地適合於不同的用途。美國能源部(DOE)科學辦公室的同位素計劃繼續支持各種放射性同位素的生產研究,以增加未來基於放射性同位素的治療方法的選擇數量。
鈾的同位素鈾-230的情況就是如此。研究人員開發了一種方法,通過"靶向α療法"使鈾-230可用於治療疾病,這是一種使用α發射同位素來治療疾病的方法。這些同位素被「拴在」生物兼容的化合物上,製成放射性藥物或"放射性藥物",可以安全地注入人體並直接輸送到腫瘤中。在美國能源部同位素計劃下生產的α發射同位素的其他例子,顯示出有希望用於定向α治療,包括錒-225和鉍-213。
鈾-230的生產始於將自然界中大量存在的釷金屬作為釷-232置於高能質子束中。在這個過程中,一些天然釷被轉化為同位素proactinium-230。Proactinium-230衰變為鈾-230,後者進一步衰變形成釷元素的同位素,釷-226。這兩種同位素,鈾-230和釷-226,都有可能被用於放射性藥物。
從壽命較長的母體同位素鈾-230的衰變中提供短壽命的釷-226子體的裝置被稱為"發生器"。一個發生器使用簡單的、不同的化學步驟將母體和子體干淨地分開,這為放射性藥物開發的下一步提供了持續的供應。
美國能源部同位素計劃的研究人員現在正致力於擴大鈾-230的生產規模,以使這兩種同位素都能廣泛使用,作為潛在的治療劑進行更廣泛的評估。
來源:cnBeta
為什麼有些免疫細胞更擅長殺死癌細胞?
免疫T細胞,依靠表面的T細胞受體(TCR)識別並攻擊體內的病毒和異常細胞,例如癌細胞。然而,滲透到腫瘤組織中的T細胞表現不盡相同,有些擅長攻擊癌細胞,有些卻反應遲鈍,甚至毫無反應。 ...
「納米分子飛彈」來了 癌細胞哪里逃
世間萬物皆有規律,哪怕是小到一個細胞,也有規律可循。一個細胞變為兩個細胞,兩個細胞變為4個細胞……人體內所有細胞都是經過這樣的分裂過程產生的。在正常情況下,人體能夠精準控制體內的細胞分裂過程——哪些細胞應該分裂,分裂什麼時候開始,什麼時候結束,分裂進行幾次,這些都需要遵循嚴格的秩序。
從左至右分別為論文共同通訊作者李洋、論文共同第一作者邵喜明、論文共同通訊作者李紅昌、論文共同通訊作者喻學鋒。
黑磷納米材料阻斷細胞有絲分裂的分子機制。中國科學院深圳先進院供圖
然而,當癌症發生時,少數細胞擺脫了這些規則的約束,開始無休止地分裂,最終在本不該發生細胞增殖的部位,產生大量細胞聚集,即表現為腫瘤。細胞分裂失控,是腫瘤不斷增殖的重要原因,因此減緩甚至抑制細胞分裂,被認為是腫瘤治療的最有效策略之一。
前不久,中國科學院深圳先進院的研究團隊發現,一種名為黑磷納米的材料,可以影響細胞分裂的進行,進而為腫瘤納米藥物的研發,提供了新思路。
8月5日,中國科學院深圳先進院李紅昌團隊、喻學鋒團隊和李洋團隊等合作完成的這項研究成果,發表於國際學術期刊《自然—納米技術》。李紅昌課題組副研究員邵喜明和研究助理丁智昊為論文並列第一作者,李紅昌、喻學鋒和李洋副3位研究員為論文共同通訊作者,中國科學院深圳先進技術研究院為第一作者單位和通訊作者單位。
李紅昌說,在過去幾十年,基於納米技術的藥物研發已經被廣泛開展。在抗腫瘤領域,納米藥物可以提供更好的靶向性和優異的藥學性質,因此被寄予厚望。但是,目前已有的納米藥物,大都屬於納米載體藥物,這種藥物只是對傳統藥物的改良,納米材料在其中僅僅充當了藥物載體的功能。
「如果把納米藥物整體比作一個膠囊,納米材料其實只發揮了『殼』的作用。納米材料能否上升到『核心藥物』的地位,關鍵在於能否發現具備詳細生物機制和明確成藥機理的納米材料。」李紅昌說。
在此次研究中,研究團隊選取黑磷納米材料為研究對象,通過精細的細胞生物學和分子生物學研究,發現納米材料在細胞內能夠精準靶向特定生物分子,並獲得獨特的生物效應,藉此提出了以分子細胞生物學機制為依託的納米精準分子靶向藥物概念,為納米藥物研發開辟新路徑。
邵喜明介紹,作為一種由單一磷元素構成的新型納米材料,黑磷具有獨特的分子結構和界面特性,在多個領域具有應用潛力。此前,研究團隊已經發現黑磷具有較高的生物活性和生物可降解特性,在腫瘤治療等生物醫學領域具備良好的應用潛能。
然而,黑磷作為一種無機納米材料,能否在分子細胞層面與生命系統產生相互作用尚不得知。在此次研究中,研究團隊發現,黑磷納米材料就像「納米飛彈」一樣,可以影響細胞分裂的進行,並以此為機制抑制腫瘤細胞增殖。
基於這項發現,團隊提出了腫瘤精準靶向「納米磷療」的新概念,為未來基於黑磷開發新型腫瘤治療藥物,奠定了科學基礎。
邵喜明說,研究團隊首先使用低濃度黑磷納米材料處理細胞,發現黑磷導致細胞周期停滯在有絲分裂期。隨後,團隊對這一現象背後的機理進行了深入挖掘,發現黑磷破壞了細胞有絲分裂核心機器——紡錘體的組裝。這一機制被最終確定為黑磷導致細胞分裂停滯的直接原因。
「同生物體內其他生命過程一樣,細胞分裂需要眾多生物分子的參與,其中PLK1激酶是非常關鍵的分子開關,其主要功能是控制紡錘體的組裝和運行。」李紅昌說。
據他介紹,黑磷進入細胞後,通過偽裝成PLK1的作用底物,吸引了大量PLK1蛋白與之結合,並使這些PLK1活性喪失,進一步造成紡錘體錯誤組裝,最終阻斷了細胞分裂的正常進行。
邵喜明說,基於這一機制,黑磷納米材料被賦予了基本的抗腫瘤藥物性質。在隨後的動物實驗中,研究團隊利用小鼠荷瘤模型,進一步證實了黑磷具備抗腫瘤效果。
磷是自然界中普遍存在的一種非金屬元素,也是地球上所有生命形式的重要組成成分。研究磷和生命系統之間的相互作用對理解生命規律以及生命進化都有重要意義,但是相關研究工作的開展需要橫跨「材料學」和「生物學」兩個一級學科,因此對研究團隊的學科背景提出了很高要求。
在此次研究過程中,研究團隊發揮了學科交叉的特色,自發組成了一支材料學與生物學交叉研究隊伍,成功讓「材料」與「生物」發生深度融合。
比如,研究團隊中的喻學鋒課題組,對黑磷納米材料進行了6年的系統研究,已經建立了完整的黑磷基納米材料的制備和應用體系,在研究過程中主要負責納米黑磷的制備和性能研究;李紅昌課題組,則精通細胞分裂機制和抗腫瘤藥物研發,在研究中主導納米黑磷的生物機制研究;李洋課題組具有豐富的納米生物學研究經驗,在研究過程中,提供符合研究方向和適用於交叉研究團隊的新思路,起著「思路潤滑」的作用。
「在實際研究過程中,單個課題組很難做到『既懂材料,又通生物』,因此對類似橫跨多個學科的課題,往往難以持續深入地進行,大多研究只能是『淺嘗輒止』。」李紅昌說。
他告訴記者,通過「材料人」和「生物人」之間不停地「思想碰撞」和持續地「互通有無」,項目組最終發現了無機單質納米磷材料影響細胞分裂的重要現象,並深入解析了背後的分子細胞機制,這也是中科院深圳先進院堅持「學科交叉」理念和秉承「面向世界科技前沿」導向而產生的又一個代表性科研成果。
來源:cnBeta
臭臉但是心地非常好! 大橘每天「步行1.6公里」到醫院:準備上班~
千萬不要「以貌取人」!英國諾森伯蘭郡(Northumberland)有一隻10歲的橘貓Yang。從4年前開始,牠每天都會走約1.6公里的路程,去赫克瑟姆綜合醫院「上班」。天氣好的時候,牠會在吃完早餐後出發,下午6、7點回家;如果下雨的話牠就「休假」。
▼去醫院的路,Yang已經走得很熟了。牠每天沿著街坊的後院走到主幹道上,還懂得等綠燈亮了再過馬路。
▼到醫院後,Yang會在門口等一會兒,跟病人們打招呼,然後再走進大樓巡邏。如果上班累了,牠就在救護車上睡午覺。
▼Yang的主人是48歲的Glynis Bell,她表示愛貓從小時候就喜歡出去冒險,以前還經常去火車站。Yang養成去醫院的習慣,還要從一次巧合說起。那次Bell要回老家待幾天,就拜託一位朋友2天來餵一次貓咪。但Yang跟這位朋友相處得很不好,牠乾脆離家出走,跑去家附近的醫院住。一來而去牠竟然喜歡上了醫院,現在每天都要去報到。
▼醫院把Yang當成非官方吉祥物,患者們看到牠也非常開心。Yang好像能感知病人的痛苦,牠尤其關心在醫院接受化療的癌症患者,還會用爪子輕輕拍他們的膝蓋,好像在問:「今天有感覺好一些嗎?」
https://twitter.com/GemmaR_1986/status/1215223524954181632
▼6個月前,Yang突然撞擊Bell的胸口。剛開始Bell不明白牠為什麼這樣做,沒想到幾週後竟然查出了心臟病。原來Bell是在提醒她,注意自己的心臟!
Yang非常聰明,能對病人的痛苦感同身受,還會看病,難道牠上輩子是醫生?這個小天使太可愛了!
來源:網路資料
來源:花生時報wwwallother
新發明的的尿液或血液測試方法可以發現腦腫瘤
來自劍橋大學的醫學研究人員開發了兩種新的測試方法,能夠檢測膠質瘤的存在,這是一種腦瘤。使用新開發的測試可以在病人的尿液或血漿中檢測到腫瘤,這也是世界上第一個此類測試方式。
研究人員在他們的論文中明確表示,新的測試方法還處於試驗的早期階段,目前只分析了少量的病人。盡管樣本量很小,但該小組表示,結果是有希望的。這些結果表明,在未來,醫生可以用測試來監測有腦瘤風險的病人。
新方法能夠通過血液測試和尿液測試來監測病情,比每三個月做一次核磁共振檢查要方便得多,這是目前的標準測試方法。雖然一些腦瘤可以被切除,但腫瘤復發的可能性也很高。由於復發的發生率很高,已經從大腦中切除腫瘤的人每三個月進行一次核磁共振成像監測,然後再進行活檢。
由於這些測試非常復雜,檢測不同癌症類型的血液測試就成為各路醫學研究的一個重要焦點。有一些檢測癌症的血液測試在臨床上使用。它們通常是基於發現腫瘤細胞死亡時產生的變異DNA,即所謂的無細胞DNA。然而,檢測腦瘤中的無細胞DNA是困難的,因為血腦屏障將血液和圍繞大腦和脊髓的腦脊液分開,該屏障還阻止了細胞和其他顆粒在大腦外或進入大腦。
該項目的研究人員同時致力於兩種方法,以克服檢測腦瘤細胞-前DNA的挑戰。第一種方法對以前切除過膠質瘤並做過活檢的病人有效。研究人員設計了一種腫瘤指導下的測序測試,以尋找在病人尿液、腦脊液和血漿中的細胞-DNA內發現的腫瘤組織突變。
該團隊有8名根據核磁共振成像的疑似腦瘤患者納入了他們的研究。他們在最初的腦瘤活檢時,連同腦脊液、血液和尿液樣本一起取樣。當他們知道要尋找什麼DNA鏈時,研究人員發現即使在血漿和尿液中發現的極少量的無細胞DNA中也有可能找到突變。該測試在8個CFS樣本中的7個,12個血漿樣本中的10個,以及16個尿液樣本中的10個檢測到無細胞DNA。
來源:cnBeta
科學家首次測量到系外行星大氣中的同位素
據媒體報導,一個國際天文學家團隊--包括來自馬克斯·普朗克天文研究所的科學家--成為世界上首批探測到系外行星大氣中的同位素的科學家。它涉及的是位於Musca (Fly)星座300光年外的氣態巨行星TYC 8998-760-1 b中不同形式的碳。微弱的信號是由位於智利的ESO超大望遠鏡測量到的,這似乎表明這顆行星的碳13含量相對豐富。
天文學家假設這是因為這顆行星形成於離其母恆星很遠的地方。這項研究將發表在科學雜誌《自然》上。
同位素是同一原子的不同形式,其在原子核中有著不同數量的中子。例如,有6個質子的碳通常有6個中子(碳12),但偶爾有7個(碳13)或8個(碳14)。不過這種性質並沒有改變碳的化學性質。盡管如此,同位素的形成方式不同,對當時的環境的反應也略有不同。因此,同位素在廣泛的研究領域提供了應用:從檢測心血管疾病或癌症到研究氣候變化和確定化石和岩石的年齡。
現在,來自幾個國家的天文學家發現了年輕巨行星TYC 8998-760-1 b的大氣中這些同位素之間的不尋常比例。碳主要以CO(一氧化碳)氣體的形式存在。這顆行星本身的質量約為木星的14倍,體積幾乎是木星的兩倍。因此,天文學家把它歸類為超級木星。
由論文第一作者、荷蘭萊頓天文台博士生Yapeng Zhang領導的這組科學家成功地區分了碳13和碳12。Zhang指出:「我們能在這麼遠的距離外在系外行星的大氣層中測量到這一點真的很特別。」天文學家們曾預計,每70個碳原子中就有一個是碳13,但在這顆行星上,這個數字似乎是原來的兩倍。他們的想法是,碳13含量更高,這跟系外行星的形成存在某種關聯。
Mollière解釋稱:「這顆行星到其母恆星的距離是地球到太陽的距離的150多倍。在如此遙遠的距離,冰可能已經形成了更多的碳13,並導致這種同位素在今天的行星大氣中的比例更高。」假設碳13的富集跟形成行星的原行星盤中CO的凍結有關。在這種情況下,這可能意味著太陽系的行星沒有收集到很多富含碳13的冰。一個原因可能是,在太陽系中,超出CO開始從氣相中凍結的距離即CO雪線,位於海王星軌道之外。因此,CO冰可能很少被納入太陽系的行星,從而導致較高的同位素比率。據悉,Mollière編寫了數據分析軟體並對分析結果做出了貢獻。
這顆系外行星TYC 8998-760-1 b是在兩年前由萊頓大學的博士生、這項研究的論文合著者Alexander Bohn發現。他補充道:「這一發現離『我的』行星很近,這真是太棒了。這很可能是以後許多事情的開始。」
萊頓大學教授Ignas Snellen多年來一直是這門學科的推動力量。「我們期望在未來,同位素將進一步幫助我們准確地了解行星是如何、在哪里和何時形成的。這個結果僅僅是個開始。」
來源:cnBeta
科學家開發新型基因療法 可能對多種類型的癌症有效
據媒體報導,根據7月發表在美國癌症研究協會雜誌《癌症發現》上的一篇論文,西奈山伊坎醫學院的研究人員已經開發出一種治療劑,在體外顯示出對幫助癌症生存的生物途徑的高度有效性。
該療法是一種工程分子,名為MS21,它能引起AKT的降解,這種酶在許多癌症中過度活躍。這項研究為AKT的藥理降解是治療某些基因突變的癌症提供了證據。
AKT是一種癌症基因,它編碼的酶在癌細胞中經常被異常激活以刺激腫瘤生長。AKT的降解可以逆轉這些過程並抑制腫瘤的生長。
西奈山伊坎醫學院Tisch癌症研究所所長、Ward-Coleman癌症研究主席和腫瘤學主席Ramon Parsons博士說:「我們的研究為臨床開發一種AKT降解劑以治療具有某些基因突變的人類癌症奠定了堅實基礎。對44000例人類癌症的研究發現,19%的腫瘤至少有一個這樣的突變,這表明大量的癌症患者可以從AKT降解劑(如MS21)的治療中獲益。」
MS21在人類癌症衍生的細胞系中進行了測試,這些細胞系是實驗室中用來研究癌症療法療效的模型。研究人員正在尋求與一個行業合作夥伴一起開發MS21,以便為患者開啟臨床試驗。
「將這些發現轉化為對患者有效的癌症療法是一個高度優先事項,因為我們在這項研究中闡述的突變和由此產生的癌症驅動途徑可以說是人類癌症中最常見的激活途徑,但這項工作被證明特別具有挑戰性,」西奈山伊坎醫學院治療學發現中心主任金健(音譯)博士說。「我們期待著有機會將這種分子發展成一種可以在臨床試驗中進行研究的療法。」
來源:cnBeta
新型納米粒子可對放射治療產生反應以從內部殺死癌症
據媒體報導,放射療法是目前我們對抗癌症的最佳療法之一,但它可能受益於更有針對性地保護健康細胞。現在,日本的研究人員已經開發出了一種納米粒子,它可以穿透腫瘤並在外部X射線激活後從內部殺死腫瘤。
通常情況下,放射治療通過破壞癌細胞的DNA起作用,然而這種療法一部分來自活性氧的產生。這意味著需要氧氣,而在腫瘤中心可能缺乏氧氣,這使得該種療法受到了限制。
因此在這項新研究中,來自京都大學的科學家和同事們研究了一種使用輻射殺死癌細胞的不同方式。他們設計了可以滲透腫瘤的納米顆粒,一旦進入腫瘤就可以被X射線激活,然後用另一種方法--光電效應(即一種材料對電磁輻射發出電子)--來摧毀細胞。
納米顆粒由有機矽製成並在其孔隙中攜帶碘。碘是那里的活性成分,當輻射水平相對較低時會釋放電子。這些電子隨後會導致癌細胞核DNA的雙鏈斷裂進而引發細胞死亡。
為了驗證這一想法,研究小組將納米顆粒分散到健康細胞和癌細胞的3D模型中。他們發現納米粒子傾向於聚集在癌細胞的細胞核外,30分鍾的X射線輻射足以在三天內將它們消滅。在輻射水平為33.2 keV時取得了最好的結果。
「我們的研究代表了在癌細胞內運用量子物理現象的一個重要例子,」該研究的論文合著者Kotaro Matsumoto說道,「這似乎在DNA附近產生了低能電子雲並導致難以修復的雙鏈斷裂,最終導致了程序性細胞死亡。」
利用能被外界輻射激活的納米粒子來殺死癌症的基本概念並不新鮮,但它有多種形式。以前的研究已經能通過加熱、改變酸度釋放藥物或活性氧或讓它們缺乏營養的方式來使用納米顆粒從內部殺死癌症。現在看來,釋放電子可能是武器庫中的一種新武器。
目前這項研究還處於早期階段。這項技術只在實驗室培養的細胞中進行過測試,還沒有在動物身上進行過測試,更不用說在人類身上了。研究人員表示,他們接下來的工作是對老鼠進行測試。
來源:cnBeta
研究稱2020年全球超過74.1萬例癌症病例與飲酒有關
一項新研究表明,酒精和癌症風險是緊密相連的。研究人員得出結論,去年超過74.1萬例癌症診斷可能與飲酒有關。這超過了去年新診斷的癌症患者總數的4.1%。該研究表明,經常飲酒和大量飲酒是可能導致癌症的危險行為。但即使是適度飲酒,也足以導致每年多達10萬個病例。
研究人員發現,男性比女性更有可能得到與酒精有關的癌症診斷。他們還將中歐、東歐和亞洲的特定國家與酒精相關癌症的風險增加聯系起來。然而,隨著某些地區酒精使用的轉變,與酒精有關的癌症的地理分布可能會出現重大變化。
在這項研究中,作者研究了2010年全世界的酒精飲用情況。他們假設在診斷前有10年的潛伏期。然後他們計算了去年有多少新病例可以歸因於某種形式的飲酒。
癌症風險隨著飲酒的增加而增加
飲酒的男性的癌症風險明顯高於女性。在74.1萬個病例中,大約75%是飲酒的男性。
研究人員說,最常見的癌症涉及食道、肝臟和乳房(女性)。他們發現,加上胃癌和胰腺癌,2020年的癌症診斷數字增加到80.8萬以上。在敏感度分析中,作者考慮了以前的飲酒情況,使病例數增加到近92.6萬。
作者還研究了每日酒精攝入量和癌症風險。他們發現,大量飲酒者更有可能在未來面臨癌症診斷。但即使是較少的飲酒量也是癌症發展的一個風險因素。每天喝一兩杯酒可能足以導致超過10萬個癌症病例。
該研究說,飲用少於20克的酒精(兩杯酒精飲料)就會轉化為中等程度的癌症風險。他們把每天使用多達60克酒精的情況標為危險飲酒。他們說,每天超過60克相當於酗酒。
酗酒者的癌症診斷率最高,超過346,000。即使是每天只喝10克酒精的人,10年後也有患癌症的風險。研究中約有41,000個病例是由於每天只喝了一杯酒精飲料而導致的。
研究指出,「男性每天飲酒30至40克以下和40至50克以下,女性每天飲酒10至20克以下和20至30克以下,酒精導致的癌症發生頻率最高」。
酒精使用趨勢的變化
科學家們承認,近年來飲酒趨勢出現了令人鼓舞的下降,但其他地區可能會出現大幅增長。作者總結說,衛生官員需要做更多的工作,讓公眾了解未來的酒精使用和癌症風險。
我們的研究結果突出表明,需要採取有效的政策和干預措施,提高對與飲酒有關的癌症風險的認識,減少總體酒精消費,以防止酒精所致癌症的負擔。
該研究還表明,「經過嘗試和測試的稅收政策已經導致中歐和東歐的人口酒精消費減少,可以在世界其他尚未制定有效酒精政策的地區實施」。
來源:cnBeta
MIT科學家開發納米粒子尿液測試 可診斷癌症並確定其位置
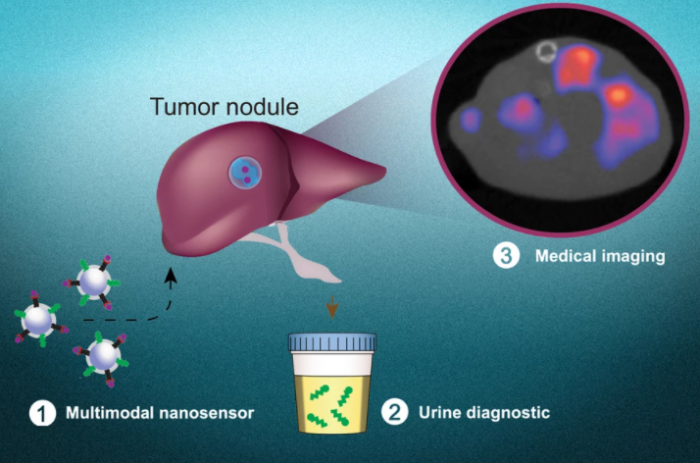
據媒體New Atlas報導,麻省理工學院(MIT)的研究人員已經開發出了納米粒子,可以通過尿液測試來揭示癌症,並在後續工作中准確定位其在體內的位置。癌症發現得越早,對病人的治療效果越好。現在,MIT的研究人員開發了一種新的診斷系統,可以作為一種簡單的尿液測試來檢測癌症的存在,如果呈現陽性結果,後續測試可以定位它在身體中的位置。
MIT的系統是圍繞著一種特別設計的納米粒子建立的,如果一個人患有癌症,它可以在尿液中產生「合成生物標志物」,而且在以前的測試中,它被證明在這項工作上很有希望。但問題是,它無法知道腫瘤在身體的哪個部位。現在,該團隊已經增加了這項功能。
納米粒子檢測癌症的方法是相當聰明的。為了逃離它們的起源點並擴散到整個身體,許多癌症使用稱為蛋白酶的酶來切割細胞外基質中的蛋白質。診斷用的納米粒子表面塗有肽,這些肽也能被這些蛋白酶切開,所以如果某處有腫瘤存在,納米粒子在到達尿液時就會留下它們遭遇的「傷痕」。
知道是否患有癌症和知道它在哪里是兩個非常不同的問題,因此為了幫助回答第二個問題,該團隊調整了納米粒子的配方。他們添加了一種肽,這種肽被酸性環境所吸引,就像腫瘤在自身周圍產生的那些環境一樣,這意味著納米粒子傾向於聚集在癌症周圍。他們還添加了銅-64,一種在PET成像下發光的放射性示蹤劑。
這意味著納米粒子將聚集在腫瘤部位,並在PET掃描下清晰可見。該團隊說,這種方法使腫瘤比常用的PET示蹤劑更突出,後者還能使心臟等器官發出強烈的光芒,並可能沖掉附近的任何癌症信號。
該團隊在患有轉移性結腸癌的小鼠身上測試了這些顆粒,並能夠跟蹤它們對化療的反應。從長遠來看,如果它被用於人類,研究人員設想該測試將成為年度健康檢查的一部分。
該研究的主要作者Sangeeta Bhatia說:「每年你都可以進行一次尿液測試,作為一般檢查的一部分。只有當尿檢結果呈陽性時,你才會進行成像研究,然後找出信號的來源。我們在科學上還有很多工作要做,但從長遠來看,這就是我們想去的地方。」
這項研究發表在《自然材料》雜誌上。
來源:cnBeta
研究發現帕金森病、癌症和2型糖尿病共享一個驅動疾病的關鍵因素
據媒體報導,當細胞受到壓力時,化學「警報」就會響起,啟動一系列的活動,保護細胞最重要的角色。在這一過程中,一種叫做Parkin的蛋白質急於保護線粒體,即為細胞產生能量的「發電站」。現在,索爾克研究所研究人員已經發現了細胞壓力的一個主傳感器和Parkin本身之間的直接聯系。同樣的途徑也與2型糖尿病和癌症有關,這可能為治療這三種疾病開辟了一條新途徑。
「我們的發現代表了人們所發現的Parkin的警報反應中最早的一步,這是一個很大的挑戰。所有其他已知的生化事件都是在一小時內發生的;我們現在發現了在五分鍾內發生的事情,」美國國家癌症研究所指定的索爾克癌症中心主任、這項新工作的資深作者 Reuben Shaw教授說。這項工作已發表在2021年4月7日的《科學進展》。「對細胞處置有缺陷的線粒體的方式的這一主要步驟進行解碼,對一些疾病有影響。」
Parkin的工作是清除因細胞壓力而受損的線粒體,以便新的線粒體能夠取而代之,這一過程稱為有絲分裂。然而,Parkin在家族性帕金森病中發生了突變,使得該蛋白無法清除受損的線粒體。雖然科學家們已經知道Parkin以某種方式感知線粒體壓力並啟動有絲分裂過程,但沒有人確切了解Parkin是如何首先感知線粒體的問題的--Parkin以某種方式知道在線粒體受損後遷移到線粒體,但在Parkin到達那里之前,沒有已知的信號。
Shaw的實驗室因其在新陳代謝和癌症領域的工作而聞名,他們花了數年時間深入研究細胞如何調控一個更普遍的細胞清潔和回收過程,即自噬。大約十年前,他們發現一種叫做AMPK的酶,對多種細胞壓力(包括線粒體損傷)高度敏感,通過激活一種叫做ULK1的酶來控制自噬。
在這一發現之後,Shaw和研究生Portia Lombardo開始尋找由ULK1直接激活的自噬相關蛋白。他們篩選了大約50種不同的蛋白質,預計約有10%的蛋白質適合。當Parkin在名單上名列前茅時,他們感到非常震驚。生物化學途徑通常是非常復雜的,涉及多達50個參與者,每個參與者都會激活下一個。發現像有絲分裂這樣重要的過程只由三個參與者啟動--首先是AMPK,然後是ULK1,然後是Parkin--是如此令人驚訝,以至於Shaw幾乎無法相信它。
為了證實這些發現是正確的,研究小組使用質譜儀精確地揭示了ULK1在哪里將一個磷酸基團附著在Parkin上。他們發現,它落在一個新的區域,其他研究人員最近發現它對Parkin的激活至關重要,但不知道為什麼。Shaw的實驗室的一名博士後洪建民隨後進行了精確的生化研究,以證明時間線的每一個方面,並劃定了哪些蛋白質在做什麼,在哪里做。Shaw的研究現在開始解釋Parkin激活的這個關鍵的第一步,Shaw假設這可能是AMPK通過ULK1向Parkin發出的一個 "提示 "信號,即在第一波損傷後去檢查線粒體,並在必要時觸發對那些嚴重受損無法恢復功能的線粒體的破壞。
這一發現具有廣泛的意義。AMPK是細胞新陳代謝的中心傳感器,它本身被一種叫做LKB1的腫瘤抑制蛋白激活,該蛋白參與了一些癌症,正如Shaw在之前的工作中所確定的那樣,它被一種叫做二甲雙胍的2型糖尿病藥物激活。同時,許多研究表明,服用二甲雙胍的糖尿病患者表現出較低的癌症和衰老並發症的風險。事實上,二甲雙胍目前正作為首批 "抗衰老 "治療藥物之一進行臨床試驗。
「對我來說最大的收獲是,新陳代謝和線粒體健康的變化對癌症至關重要,對糖尿病至關重要,對神經退行性疾病也至關重要,」擔任 William R. Brody Chair主席的Shaw說。「我們的發現表明,一種激活AMPK的糖尿病藥物--我們之前表明它可以抑制癌症,也可能有助於恢復神經退行性疾病患者的功能。這是因為支撐我們身體內細胞健康的一般機制比任何人想像的都要綜合得多。」
來源:cnBeta
WHO警告:即便是少量飲酒也會增加患癌風險
據媒體報導,世衛組織(WHO)近日發表了一項新的研究,該研究表明適度飲酒跟患某些癌症的風險顯著增加有關--其中包括結腸癌和乳腺癌。這項研究來自世衛組織的國際癌症研究機構(IARC),該機構還發現,輕度飲酒者也存在風險增加的情況。
據悉,這項新研究主要集中在加拿大。去年,加拿大的研究人員將酒精攝入跟1/7的新癌症病例聯系在一起。研究人員稱,在跟飲酒有關的7000例病例中,24%為乳腺癌,20%為結腸癌,15%為直腸癌,13%為肝癌和口腔癌。
輕度和中度飲酒--即每天飲酒不超過兩杯--對健康構成的風險一直是一個有爭議的話題。最近幾個月的許多研究表明,這種類型的飲酒跟從心臟到大腦健康的風險增加有關。
這項新研究的研究人員表示,所有的飲酒都有風險,至少在關注跟酒精有關的癌症時是這樣。研究合著者Jurgen Rehm博士稱,比如每天一杯葡萄酒就會使女性患乳腺癌的風險增加6%。
另一項研究的合著者Kevin Shield博士詳細闡述了飲酒是如何增加患幾種癌症的風險的:「酒精會以多種方式導致癌症。酒精導致癌症的主要機制是破壞DNA修復。其他途徑包括慢性飲酒導致肝硬化、酒精導致性激素失調、導致乳腺癌。酒精還會增加吸菸者患頭頸癌的風險,因為它會增加菸草致癌物的吸收。」
鑒於新冠大流行期間報告的酒精消費量大幅上升,這些發現尤其令人擔憂,因為過去的研究發現,許多人在封鎖期間開始喝更多的酒。
來源:cnBeta
慢性肺病損害的細胞可導致嚴重的COVID-19症狀
由由轉化基因組學研究所(TGen)領導的一項國際研究的結果表明,SARS-CoV-2利用了預先存在的肺部疾病患者的基因變化。研究結果表明,慢性肺部疾病患者的氣道做好了被COVID-19病毒感染的"預備工作",帶來了更嚴重的症狀、更差的預後和更大的死亡可能性。
這項研究今天發表在《自然-通訊》上,它詳細介紹了慢性肺部疾病引起的各種細胞分子構成的基因變化,包括襯托肺部和氣道的上皮細胞。該研究詳細說明了這些變化如何幫助使SARS-CoV-2(引起COVID-19的病毒)進入人體,進行復制並引發失控的免疫反應,使肺部充滿液體,並經常導致患者需要呼吸機和長時間住院治療。
研究小組利用單細胞RNA測序技術,從各種資料庫中拼出了611398個細胞的遺傳密碼,這些細胞既代表了健康(對照)肺部,也代表了慢性肺部疾病的患者。測序和分析使研究人員能夠確定可能導致COVID-19結果惡化的分子特徵。
TGen綜合癌症基因組學部副教授、該研究的資深作者之一Nicholas Banovich博士說:"我們的結果表明,慢性肺部疾病患者在分子上更容易受到SARS-CoV-2感染。"Banovich博士是人類細胞圖譜肺部生物網絡的主要參與者,該網絡的幾十名成員代表全球80多個機構,也為這項研究做出了貢獻。
此外,老年、男性、吸菸以及高血壓、肥胖和糖尿病等合並症,都是COVID-19的風險因素,而慢性肺部疾病,如慢性阻塞性肺病(COPD)、間質性肺病(ILD),尤其是特發性肺纖維化(IPF),是肺部組織的漸進性結疤和僵化,都會使COVID-19的風險加劇。
范德比爾特大學醫學中心醫學和細胞與發育生物學副教授、醫學博士Jonathan Kropski說:"在大流行的早期,人們就認識到慢性肺部疾病患者患嚴重COVID-19的風險特別高,而我們的目標是深入了解造成這種情況的細胞和分子變化,"他是該研究的共同第一作者。
肺部細胞和免疫細胞的變化
研究人員特別搜索了AT2細胞(一種主要的肺上皮細胞類型)的變化,重點關注與COVID-19相關的細胞途徑和基因表達水平。他們建立了一個 "病毒進入得分",即與SARS-CoV-2相關的所有基因的綜合得分,並發現慢性肺部疾病患者的細胞得分更高。
他們還探索了免疫細胞的變化,發現了與過度炎症和持續細胞因子產生有關的基因表達失調,這是嚴重SARS-CoV-2感染的兩個標志性症狀。COVID-19患者中所謂的細胞因子風暴釋放出一連串的免疫細胞,淹沒了肺部,造成嚴重的器官損傷。
該研究的主要作者之一、Banovich博士實驗室的博士後Linh Bui博士說:"免疫細胞的基因變化,特別是被稱為T細胞的特化白細胞,可能會削弱病人對病毒感染的免疫反應,導致慢性肺部疾病患者出現嚴重疾病和不良後果的風險更高。我們的數據表明,被慢性疾病破壞的肺部在分子和細胞水平上的免疫微環境可能造成COVID-19重症病例。
來源:cnBeta
研究:74.1萬例新癌症病例被發現跟飲酒有關
據媒體報導,國際癌症研究機構(IARC)的一項新研究估計,去年約74萬例新診斷的癌症病例可以歸因於飲酒。該研究呼籲加強公共衛生戰略以提高人們對酒精和癌症之間聯系的認識。癌症風險增加跟飲酒之間的聯系早已為人所知。 2018年,劍橋大學的一個研究團隊發表了一項里程碑式的研究,該研究專注於酒精如何損害DNA並為解釋其中的因果機制提供了一些初步線索。
資料圖
當然,很難將飲酒跟癌症直接聯系起來。由於存在諸多混雜因素,要准確量化有多少癌症病例可以直接歸因於飲酒是一項挑戰。
現在這項新研究則通過比較2010年收集的人均酒精攝入量數據和2020年報告的新癌症病例提供了最新的估計。研究結果估計,2020年74.13萬例新發癌症病例可能跟飲酒有關,其約占全球新發癌症病例的4%。
酒精和癌症之間的聯系還會因地理位置的不同而有很大的不同。在中國,6%的新癌症病例可能與飲酒有關,而在美國,只有約3%的新病例可能跟飲酒有關。
國際癌症研究機構的Harriet Rumgay報告稱:「趨勢表明,盡管許多歐洲國家的人均酒精消費量有所下降,但在中國和印度等亞洲國家及撒哈拉以南非洲國家酒精消費量卻在上升。」
其中,男性占所有酒精相關癌症病例的3/4。食道癌、肝癌和乳腺癌最常跟飲酒有關。此外,雖然酗酒占了大部分病例,但在所有跟酒精有關的癌症中有1/7跟適量飲酒有關。
「我們的研究強調了即使相對較低水平的飲酒對癌症發病率的貢獻也令人擔憂,不過也表明,公共飲酒行為的微小改變可能會對未來的癌症發病率產生積極影響,」Rumgay說道。
研究人員清楚地注意到了這類分析的局限性。如這項研究沒有說明酒精和菸草攝入之間的關系,這兩種致癌物質通常都是協同攝入的。
然而該研究確實表明,它的結論是基於商業銷售數字的人均酒精消費量的保守估計。約1/4的全球酒精消費被認為是在商業記錄的銷售數據之外發生的,所以我們假設目前的研究結果更有可能低估了酒精對癌症的總影響。
Rumgay表示,這項新研究最重要的成果是提高了人們對酒精和癌症之間關系的認識。她建議採取一些基於政策的公共衛生干預措施以此來幫助減少跟酒精有關的癌症的全球負擔。
Rumgay說道:「公共衛生策略如減少酒精的供應在酒精產品上貼健康警告標簽及市場禁令可以降低酒精導致的癌症的發病率。導致歐洲酒精攝入量減少的稅收和定價政策--包括提高消費稅和最低單位定價--也可以在世界其他地區實施。」
來源:cnBeta
研究:保護性蛋白質TRPM7可防止癌細胞擴散到血液中
據媒體報導,當癌症擴散到全身時它會變得更加危險。現在,來自約翰霍普金斯大學的研究人員已經發現了一種阻止細胞進入血液的蛋白質,另外他們還發現轉移的癌細胞忽略了它。這些可能為癌症治療揭示一個新的藥物靶點。 癌症的主動性無疑是令人沮喪的。當它在身體的某個部位站穩之後,它往往會開始脫落一些流氓細胞,這些細胞冒險則會進入血液然後轉移到其他器官進而建立一個新的「殖民地」。這種轉移過程使得癌症更難追蹤和清除,也因此更加致命。
於是,尋找預防轉移的方法成為了癌症研究的一個主要部分。近年來,科學家們發現了有助於腫瘤擴散的分子、蛋白質和蛋白質信號通路,這為開發針對這些分子的藥物提供了良好的起點。現有的一種藥物已經被發現可以修補癌細胞更容易穿透的滲漏血管。使用納米顆粒包裹免疫細胞可以幫助它們追蹤血液中的流氓癌細胞,或改變飲食可以幫助減少轉移的機會。
在這項新研究中,研究人員發現了一種蛋白質,它可能能成為預防轉移的新的潛在藥物靶點。研究人員早就知道它可以調節細胞中的鈣水平,但他們現在發現,這種蛋白質還有另一種功能,即可能在轉移中發揮作用。
該研究的首席作者Kaustav Bera表示:「我們發現,這種名為TRPM7的蛋白質能夠感知循環系統中液體流動的壓力並阻止細胞在血管系統中擴散。我們發現轉移性腫瘤細胞顯著降低了這種傳感器蛋白的水平,這就是它們能有效地進入循環而不是離開液體流動的原因。」
有趣的是,健康細胞的TRPM7含量比腫瘤細胞高得多,這就很好地解釋了為什麼癌症更容易擴散。
研究小組還發現,細胞在一種類似階梯的微通道血流模型中移動,另外血流被精心控制。他們發現,健康的成纖維細胞會因液體流動而改變方向,但會進入液體靜止的通道。
接下來,研究人員阻止了細胞表達TRPM7蛋白--果然,這次它們忽略了液體的流動、直接進入了那些快速流動的通道。相反,當它們編輯腫瘤細胞以表達更多的蛋白質時又對液體流動變得敏感了。
雖然目前這一研究還處於早期階段,但最新的發現可能為一種通過靶向TRPM7蛋白來預防癌症轉移的新療法鋪平了道路。
該研究的資深作者Konstantinos Konstantopoulos指出:「在將其應用於臨床之前,我們還需要進一步的研究進展,但我們相信,我們首次提供了TRPM7在腫瘤轉移的關鍵步驟中所起作用的明確圖像。」
來源:cnBeta
揭開腸道菌抗腫瘤的機制:微生物短鏈脂肪酸改善癌症的過繼免疫療法
人類腸道中大量的細菌——被認為與慢性炎症腸道疾病的發展有關,引發糖尿病,導致肥胖,甚至神經系統疾病,如多發性硬化症和帕金森氏症都可能有其原因,更不用說抑鬱症和孤獨症了。據估計,每個人的消化道中大約有 100 萬億個細菌細胞,它們屬於幾千種。
自一項新技術——高通量測序——實現了快速精確地分析這些細菌,微生物組一直是 20 年來的研究重點。從那時起,有越來越多的發現表明,微生物組,有時也被稱為人類第二基因組,不僅對消化具有核心重要性,而且影響,如果不是控制,至少是大量的身體功能。免疫系統被特別頻繁地提到。
免費索取人源化小鼠資料領 取
腸道微生物群已被證明能直接影響特定癌症免疫療法的療效。特別是免疫檢查點抑制 (ICI) 治療和使用腫瘤特異性 CD8 +細胞毒性 T 淋巴細胞 (CTL) 的過繼細胞治療會受到腸道微生物群組成的影響。最近,幾項研究表明,腸道微生物群的成員能夠增強 PD-1 和 CTLA4 阻斷療法的抗腫瘤功效 。Akkermansia muciniphila 和一些雙歧桿菌菌株已被證明可以調節抗腫瘤免疫反應並改善 ICI 治療。此外,由...
新型癌症療法:利用生物可降解納米粒子來關閉癌細胞「發電站」
想像一座由一組發電站供電的城市。如果所有的電站同時關閉將會造成全市范圍的停電。城市將陷入停滯,混亂可能隨之而來,但最重要的是,城市將無法發揮應有的功能。我們身體的每個細胞都可以看作是一個小城市。
細胞中沒有建築物,而是有細胞核和核糖體等細胞器。細胞的「發電站」是線粒體,它以三磷酸腺苷(ATP)的形式產生燃料。如果線粒體突然關閉,細胞就會面臨死亡--無論是健康細胞還是癌細胞。
這正是Jan van Hest和他的研究團隊跟來自中國和英國的研究人員合作的一種新型癌症治療方法,即光動力療法(PDT)的目的。Jan van Hest目前正領導著TU/e的復雜分子系統研究所(ICMS)。
光動力治療
PDT是一種無毒和無創的替代現有的治療方法以此來消除癌細胞,如化療、放療和選擇性手術。對於患者來說,這些治療可能會產生許多副作用、影響他們的生活質量,但幸運的是,不那麼粗糙的選擇正在開發中。
在光動力療法中,病人會被注射帶有光敏劑(一種對光起反應的材料)的微小納米顆粒。當納米顆粒聚集在癌細胞附近時,它們會被雷射照射並產生一種特定形式的氧氣,這種氧氣對癌細胞有毒並最終導致癌細胞死亡。
在TU/e中,Jan van Hest和他的研究小組在改進PDT方法方面取得了穩步進展,去年,他們就在《ACS Nano》上發表了一項研究。
關閉癌細胞
然而,通過設計PDT納米顆粒進入癌細胞並破壞其供電線粒體,細胞可以迅速「斷電」,PDT治療的有效性將大大提高。換言之,納米顆粒可以以更有針對性和更快的方式殺死癌細胞。
van Hest說道:「這項研究的主要挑戰是弄清楚如何將PDT納米顆粒進入癌細胞,並在進入細胞之後將納米顆粒引導到線粒體。一旦靠近線粒體,這些納米顆粒的光敏劑就會被光激活進而污染線粒體的微環境、關閉細胞最重要的電源供應。」
螢光的重要性
該團隊開發了一種將納米顆粒製成生物可降解聚合體的方法,這種空心球體可以攜帶藥物、蛋白質或光敏劑。
然而,跟以前的納米顆粒不同的是,新版本的納米顆粒被設計成在組成它們積木組裝時發出螢光。
這種螢光過程被稱為聚集誘導發射,發射響應會使得追蹤納米顆粒在組織中的位置變得更容易。
為了快速將納米顆粒導向細胞內的線粒體,該團隊將吡啶分子附著在納米顆粒的表面。一旦納米顆粒在線粒體聚集,它們的光敏劑就會被雷射激活從而有效地毒害癌細胞的微環境。這項新研究已經成功地在體內和體外實驗中證明了這一過程。
對未來治療的考慮
盡管如此,van Hest還是很快指出,雖然PDT是一種革命性的新型非侵入性治療方法,但仍需要其他治療方法。「這項工作是開發有效PDT納米顆粒的下一步。作為一種治療方法,它將跟現有的治療方法結合起來效果最好。重要的是,它將減少對放療和化療的依賴,這只會對患者有好處。我們仍需要更有選擇性和更有效的治療癌症的方法。光動力療法在靶向和消除癌細胞方面具有選擇性和准確性的潛力。這項研究表明,我們可以有效地設計出所需的材料,從而構建出能夠殺死癌細胞的高效自組裝納米粒子。」
這些發現推動了對納米顆粒、跟蹤和功效的進一步研究和發展。但當涉及到線粒體或癌細胞「發電站」時,它們的前景就不那麼光明了。
來源:cnBeta
生命的福音:基因編輯病毒治癒癌症
摘要:用某種病毒來感染癌症患者的療法曾經引人側目——如果沒有引起醫療事故訴訟的話——但可能很快就會成為慣例。經過一個多世紀的研究,以及一些令人恐懼的實驗,這些可用於治療癌症的病毒正逐漸進入人們的視野。 來源:Discover
作者:Nathaniel Scharping
翻譯:任天
在美國波士頓的一家醫療中心里,弗蘭克·尼爾森坐在一間隔離起來的房間內,表情堅毅,准備接受第一次注射。醫生拿起一支裝滿單純皰疹病毒(herpes simplex virus,簡稱HSV)的注射器,准備直接刺入他的頭皮。如果一切順利的話,這一針可能會挽救他的生命。
尼爾森是一位癌症「倖存者」,但後來又再次成為癌症患者。他患上的是黑色素瘤,第一次常規治療雖然起了作用,但現在再次復發,而且似乎更有侵略性。幾周之內,他頭皮上的腫瘤就腫脹起來,變成難看的一團腫塊。由於腫得太快,此時已經不能再像第一次治療那樣進行手術切除。
尼爾森的醫生轉向了一種名為T-VEC的尖端藥物,作為最後的治療手段。該藥物於2015年在美國獲得批准。更確切地說,T-VEC屬於免疫療法的范疇,是癌症治療領域前景廣闊的一種藥物。T-VEC看起來一點也不像藥物,而是由一種基因改造的病毒組成,能在體內扮演戰士和偵察兵的角色:既可以直接攻擊腫瘤細胞,又能從免疫系統中召喚支援。
尼爾森的醫生希望T-VEC能與免疫治療藥物帕博利珠單抗(Keytruda)「並肩作戰」,控制住他的腫瘤。帕博利珠單抗是用於癌症免疫療法的人源化PD-1單克隆抗體,能使免疫系統識別並摧毀腫瘤細胞。
尼爾森在將近一年的時間里,每隔三周就要到醫院一次,將這種藥物注射到頭皮上的腫瘤中。回家的時候,他的頭上會纏滿帶血的繃帶,一次就診多達70針的注射也讓他倍感疼痛。每一次治療後,他都要做好忍受痛苦的准備,因為身體會不可避免地出現發燒、惡心和嘔吐,這是對突然出現的活病毒所做出的反應。
不過,痛苦的治療終於得到了回報。尼爾森表示,在第5輪治療後,他開始看到頭皮上的腫塊出現明顯的變化。對於61歲的他來說,這是一個解脫的時刻,「我沖妻子喊叫著,然後跑到臥室給她看」。T-VEC治療最終溶解了尼爾森的腫瘤,達到了單獨使用帕博利珠單抗的效果。大約兩年後,尼爾森的癌症仍未復發。
在不久的將來,可能還會有更多的癌症患者通過類似的方法使自己的病情得到緩解。用某種病毒來感染癌症患者的療法曾經引人側目——如果沒有引起醫療事故訴訟的話——但可能很快就會成為慣例。經過一個多世紀的研究,以及一些令人恐懼的實驗,這些可用於治療癌症的病毒正逐漸進入人們的視野。
高風險的初始試驗
19世紀中期,治療癌症患者的醫生開始注意到一件怪事:患有傳染病的癌症患者有時會出現腫瘤萎縮的情況。事實上,這些病例報告出來的時候,科學家們甚至都不知道病毒是什麼。例如,1896年,一位白血病患者在感染了一種可能是流感的疾病後,她的腫瘤短暫消失了,這簡直就是個奇跡。
幾十年後,研究人員開始了一項大膽的癌症治療研究:故意讓癌症患者感染各種病毒,看看它們是否有治療效果。很顯然,這種研究往往需要冒很大的風險。在1949年的一項實驗中,研究人員將肝炎病毒注射到霍奇金淋巴瘤患者體內,結果喜憂參半:7名患者的癌症出現了暫時好轉,但至少有1名患者死於肝炎。
盡管存在潛在的致命副作用,但研究人員並沒有停止試驗。對所謂「溶瘤病毒」——能感染並殺死腫瘤細胞的病原體——的研究試驗一直持續到20世紀60年代,其中就涉及了導致西尼羅病毒病、單核細胞增多症和一種腦炎的病毒。
這些實驗的理念是:病毒會進入腫瘤細胞,復制並最終將其殺死,然後再侵入其他腫瘤細胞,重復這一過程,理論上「這個過程會不斷循環往復,直到腫瘤細胞全部消失。」
許多早期溶瘤病毒試驗在今天是無法想像的,也不可能付諸實踐。在一些實驗中,科學家將感染性液體或身體組織直接注射到癌症患者體內。1974年,在日本的一項研究中,病人吃下了蘸有病毒液體的麵包片。這些試驗的參與者經常會生病,有時會很嚴重——副作用包括發燒、出血和腦部炎症等。盡管許多試驗報告稱,病毒治療有望使腫瘤萎縮,但成功總是暫時的,換言之,病毒只是暫時緩解了不可避免的結果。
對於參與了這些實驗的大多數患者來說,他們的免疫系統可能會在癌症被消滅之前就把病毒從體內清除了——如果他們沒有先被病毒殺死的話。從他們的故事中,我們可以看到溶瘤病毒的明顯缺陷:這種「藥劑」本身就是人類長期以來的勁敵。
我們現在知道,有些病毒確實會攻擊體內的癌細胞,偶爾會產生令人驚奇的效果。病毒會青睞腫瘤細胞的某些特徵,包括快速繁殖和高水平的代謝活動等。這些特徵使腫瘤細胞成為病毒的理想家園,直到病毒將其破壞並轉移至另一個細胞。
幾十年來,研究人員對這種生物關系的認識一直未能轉化為有效的癌症治療方法。他們進行了大量死亡率極高的試驗,但幾乎沒有取得真正的成功,利用病毒治療癌症的研究有所降溫。20世紀70年代,放療和化療等新的癌症療法開始成熟,給患者提供了其他選擇。多年後,科學家終於在這一領域取得了重大突破,病毒才再次回到癌症治療的前沿。
溶瘤病毒進入腫瘤細胞後,會進行復制並誘導免疫細胞前來,最終將腫瘤細胞殺死,之後病毒會轉移到其他腫瘤細胞。在健康細胞內,溶瘤病毒不會復制,也不會造成損傷
分辨敵友
2013年,美國一位名叫斯泰西·埃爾霍茲的女性因多發性骨髓瘤(一種漿細胞瘤)接受了實驗性治療。醫生向她體內注射了大量減毒的麻疹病毒。這種基因改造的病原體會瞄準腫瘤,殺死癌細胞,同時啟動患者體內的免疫系統來負責收尾工作。埃爾霍茲的癌症最終得到了完全緩解,就溶瘤病毒而言,這是一個驚人的成功案例。
不過,像埃爾霍茲這樣僅用溶瘤病毒就治療成功的病例可能只是個例。在過去十年中,研究人員已經開始將病毒和其他藥物結合使用,在更大范圍的患者中有效地治療癌症。溶瘤病毒與免疫治療藥物的結合挽救了尼爾森的生命,這可能很快就會成為治療其他多種癌症的可行方法。目前已經有數十個對癌症進行溶瘤療法的臨床試驗;近年來,隨著大型制藥公司投資或收購生物技術初創企業,許多人也對該領域產生了濃厚興趣。盡管T-VEC是迄今為止美國唯一批準的溶瘤病毒癌症藥物,但未來可能會有更多的藥物出現。
向癌症患者提供病毒浸潤麵包的日子已經一去不復返了。今天的科學家已經有能力精確地操縱病毒,也對溶瘤病毒如何工作有了更細致的理解。但最重要的,或許是一種名為「檢查點抑制劑」(checkpoint inhibitors)的開創性抗癌藥物的出現。這類藥物能促使免疫系統以癌細胞為目標,其首個藥物「Ipilimumab」於2011年獲得美國食品與藥品監督管理局批准。
研究人員發現,癌細胞在人體內的生存依賴於一種獨特的「隱身機制」,這成為一個關鍵的突破點。人體的免疫細胞會在其表面表達一種名為「檢查點」的蛋白質,而這種蛋白質通常會調節免疫系統,使其不會破壞健康細胞。當免疫細胞識別出一個檢查點蛋白時,就像啟動一個自動開關,可以使細胞停止分裂。腫瘤細胞通過顯示匹配的檢查點蛋白來利用這一機制,削弱免疫細胞的防禦能力。
檢查點抑制劑是現代免疫治療的支柱,可以阻斷免疫細胞上的這些檢查點,從而有效地消除癌細胞與它們結合的能力。這一發現為治療晚期癌症——如曾被視為不治之症的轉移性黑色素瘤——提供了可能。
當涉及防禦外來入侵者時,免疫系統主要依賴的是T細胞,它們會學會識別並殺死入侵病原體。但是,人體內並不總有足夠的T細胞來有效地完成防禦工作,這就使免疫治療藥物的成功打了折扣。於是,病毒就有了用武之地,它們會召喚更多的T細胞來到腫瘤部位。
當病毒被注入腫瘤時,腫瘤變成了受感染的組織。這些病毒能催化成群的T細胞沖向腫瘤,准備保護身體。目前,檢查點抑制劑藥物僅對一小部分患者有效,但研究人員認為,如果加入病毒的話,有效的比例可能會增加1到3倍。
這種聯合治療方法標志著癌症研究來到了重要的轉折點。2018年,由於在檢查點抑制劑方面的研究,艾利森與日本京都大學的本庶佑教授共同獲得了諾貝爾生理或醫學獎。
在免疫療法出現之前的癌症治療中,「如果你想治癒一個人,你就必須殺死每一個腫瘤細胞」,現在,醫生要做的就是為免疫系統提供工具,使其參與到抵抗腫瘤細胞的工作中。
而且,正如研究已經證明的那樣,病毒感染的有益影響會超出單個腫瘤所在的部位。實驗中發現,給小鼠注射病毒不僅能減緩目標腫瘤的生長,還能減緩身體其他部位的腫瘤生長。這是因為T細胞一旦被組織起來,就會在全身移動,在癌細胞出現的任何地方攻擊它們。研究人員將這一過程稱為對癌症的系統性免疫,而這也是全世界溶瘤病毒研究人員想要達到的目標。
給予身體抵抗腫瘤的手段,這本身就是一種非常有前景的治療方法,甚至可能用來治癒擴散迅速且致命的轉移性癌症。
人體抗癌機器
在某種意義上,尼爾森是幸運的。他頭皮上的腫瘤都緊密地聚集在一起,而且高出他的皮膚表面。這使得醫生很容易將病毒直接注入腫瘤內部。然而,有些腫瘤在人體內部,很難觸及,還有一些腫瘤會隨著轉移而遍布全身,使得治療更加困難。
目前,科學家正在研究如何應用靜脈注射的方式來實施溶瘤病毒療法。理論上,當病毒可以在全身自由移動並傳播其免疫原性信號時,即使是最難以觸及的腫瘤也可以被靶向並消滅。盡管靜脈注射在一些溶瘤病毒試驗中已經有所應用,但研究人員表示,還需要更多的工作才能使這種方法完全有效。
在癌症治療領域,更靈活的治療方法將有助於推動另一個目標的實現,即開發所謂的癌症疫苗。這些疫苗不僅能對抗腫瘤,還能將人體本身變成抗癌機器。這是一項艱巨的任務,但癌症專家們有理由對此充滿希望。目前的研究已經證明,用來建立溶瘤病毒療法的工具具有非凡的適應性。
病毒可能是世界上最好的樂高積木,你可以使用任何病毒,添加新的基因,對現有基因進行工程改造,你可以拆除,也可以重建。
利用一個小的基因突變,如今的溶瘤病毒已經可以避免感染正常的細胞。當然,科學家仍有可能對病毒進行更全面的修飾,從而創造出更精確和有效的治療方法。
研究人員正在嘗試在一種能增強免疫系統反應的病毒中加入一個基因。正如有些化學物質能刺激免疫細胞並將其引向病原體,基因改造病毒也有類似的效果。在這里,病毒被引導至已經失控的人體細胞中,這一過程可以幫助醫生在不危及患者的情況下,給予患者更大劑量的溶瘤病毒。
另一種可能的方法是,使病毒更專注於激起免疫系統的反應。這一過程被稱為「為病毒提供武器」。例如,T-VEC具有的基因修飾使其能夠表達一種化合物,人體會用這種化合物來刺激免疫系統。就像鯊魚對血液的反應一樣,免疫細胞一接觸到這些分子就會被調動起來。通過基因工程改造,可以確保溶瘤病毒被免疫系統注意到,從而對腫瘤細胞產生強烈的免疫反應。
研究人員的最終目標是讓癌症患者的身體有能力識別並對抗以往遭遇過的腫瘤,從而產生某種對癌症的免疫力。對於像尼爾森這樣的患者,這個目標的實現將是莫大的福音。現在,他們每天都必須面對癌症復發的風險,腫瘤不知在什麼時候就會死灰復燃。隨著溶瘤病毒療法的發展,癌症可能最終會與病毒感染類似——盡管令人恐懼和不安,但可以治療。
來源:cnBeta
癌症有疫苗! 首批人體實驗啟動:已有試驗者接受施打
新冠疫情在全球持續延燒,所有人都看到了疫苗的重要性。其實科學家們一直在開發各種各樣的疫苗,希望能夠打敗多種疾病。德國BioNTech就開發出了一種「癌症疫苗」,幫助人們遠離癌症。現在這種疫苗已經進入臨床試驗第二階段,首批患者接受注射。
▼BioNTech表示,這種疫苗已經足夠安全,能夠進行人體臨床實驗。罹患皮膚癌的患者注射疫苗後,還要配合處方藥Libtayo。如果治療效果比較好,對絕症患者來說不亞於重獲新生。
▼癌症疫苗的開發充滿挑戰,跟其他疫苗的試驗過程不一樣,科學家們不能給沒有罹患癌症的人注射,然後去看這種疫苗的效果。所以第一批接種疫苗的人都是3到4期皮膚癌患者。這種疫苗採用mRNA技術,透過刺激免疫系統製造抗體,從而起到保護作用。
BioNTech的聯合創始人表示,公司希望利用免疫系統本身的力量,來對抗癌症和傳染病。在跟新冠肺炎病毒的對抗中,mRNA疫苗展現出了驚人的力量,這也讓人們看到了希望。也許未來透過mRNA技術,真的能夠開發出預防癌症的疫苗呢!
來源:網路資料
來源:花生時報wwwallother
癌症免疫療法取得突破:能重新激活腫瘤抑制蛋白
據媒體報導,瑞典卡羅林斯卡學院的研究人員在癌症免疫療法的軍備競賽中取得了突破。該研究小組已經阻斷了一種可以抑制一種重要腫瘤抑制蛋白 從而使後者能重新開始工作的蛋白質。這項研究的重點是p53蛋白質,它通常被通俗地稱為「基因組的守護者」。
資料圖
這種蛋白質在細胞分裂過程中負責監視,如果它檢測到DNA損傷它就會暫停這個過程並對其展開修復,如果有問題的細胞分裂過度就會殺死它。這可以防止細胞癌變,至少這是目的所在。編碼p53的基因的突變或缺陷跟大量癌症類型有關。
一些腫瘤還可以通過一種叫做MDM2的蛋白質繞過這種細胞分裂檢查點,這種蛋白質可以使p53失效。在這項新研究中,來自卡羅林斯卡醫學院的科學家們發現,阻斷MDM2可以讓p53再次發揮其抑制腫瘤的作用。
研究小組使用了一種名為ALRN-6924的抑制MDM-2的藥物來驗證這一假設。在癌症小鼠模型中,該藥物增加了干擾素的數量--干擾素是觸發免疫系統攻擊目標的信號蛋白。因此,更多的T細胞浸潤腫瘤,p53作為檢查點警衛的功效明顯增強。在後續的測試中,研究小組還注意到從兩名人類患者身上提取的黑色素瘤具有類似的活性。
不過這最有趣的部分是p53的工作原理。我們的基因組中有一種叫做內源性逆轉錄病毒的序列,由我們從幾十萬年前祖先的感染中繼承的DNA片段組成。多達百分之八的人類基因組是由這種古老的病毒DNA組成的--p53使它們沉默以保持基因組的穩定。
然而當p53探測到癌細胞時,它會把這些序列變成武器。這種蛋白質在腫瘤內激活它們並啟動免疫系統響應以對癌症發起攻擊。研究人員認為,利用這一過程可以作為一種有用的免疫治療形式。
這項研究的首席研究員Galina Selivanova教授表示:「這表明,阻止MDM2的物質和現代免疫療法之間存在協同作用,應該加以利用。對免疫治療無效的患者來說,這些藥物的結合尤為重要。如果我們能增加干擾素的水平,我們就能增加免疫療法成功的機會。」
該團隊表示,下一步將研究類似的p53激活藥物--目前這些藥物已經在進行臨床研究,其可能有助於增強干擾素。
來源:cnBeta
研究人員通過測量細胞力量發現腸上皮的折疊和移動機制
據媒體報導,人體腸道由40多平方米的組織組成,內部表面有許多類似山谷和山峰的褶皺,這樣的結構能夠增加人體對營養的吸收。另外,腸道還有一個獨特的特點,即處於一種不斷自我更新的狀態。這意味著約每5天它內壁的所有細胞都要更新一次,這樣做的目的是保證正常的腸道功能。
截止到目前,科學家們知道,這種更新可能要感謝干細胞,這些干細胞在所謂的腸隱窩中受到保護並產生新的分化細胞。然而,導致隱窩內凹和新細胞向腸峰遷移的過程尚不清楚。
現在,一個由ICREA研究教授和IBEC組長Xavier Trepat領導的國際團隊跟IRB、巴塞隆納大學和加泰隆尼亞理工大學及巴黎居里研究所的研究人員合作破解了導致隱窩採用並保持其內凹的機制以及在不失去小腸特有的折疊形狀的情況下細胞是如何向峰值移動的。相關研究報告已發表在《Nature Cell Biology》上。
據了解,研究人員利用小鼠干細胞和生物工程和機械生物學技術開發出了小腸--一種類似於峰谷三維結構的類器官並在體內重現組織功能。通過利用同一小組開發的顯微鏡技術,研究人員首次進行了高解析度實驗從而獲得顯示每個細胞施加的力的3D地圖。
另外,通過這種體外模型,研究人員們已經證明,新細胞向峰值的運動也受到了細胞自身施加的機械力的控制,尤其是細胞骨架,這是一個決定和維持細胞形狀的纖維絲網絡。
研究人員Gerardo Ceada指出:「跟之前人們所認為的相反,我們已經能確定並不是腸隱窩的細胞推動了新細胞的上升,然而正處於頂峰的細胞把新的細胞拉上來,就像一位登山者幫助另一位登山者把他拉上來一樣。」
「通過這個系統,我們發現隱窩是內凹的,因為細胞的上表面比底部有更多的張力,這導致它們採用錐形形狀。當這種情況在幾個相鄰的細胞中發生時,結果是組織折疊並產生一種峰谷交替的模式,」研究人員Carlos Perez-Gonzalez補充道。
新的迷你腸模型將允許在可重復和真實的條件下對癌症、乳糜瀉或結腸炎等疾病展開進一步研究,即干細胞不受控制的增殖或褶皺的破壞。此外,腸道類器官可以用人體細胞製造並用於開發新藥或研究腸道微生物群。
來源:cnBeta
新研究將維生素D缺乏與結直腸癌風險聯系起來
據媒體報導,基於將維生素D缺乏與結直腸癌風險增加聯系起來的長期觀察,加州大學聖迭戈分校的一項新研究發現,生活在紫外線水平較低的國家的人們通常報告結直腸癌的發病率較高。
這項新研究採用了略有不同的方法,著眼於 186 個國家/地區的全球紫外線水平。研究人員考慮了幾個混雜因素,例如皮膚色素沉著和吸菸,同時還調整了年齡。該研究檢測到結直腸癌和紫外線暴露之間存在明顯的年齡依賴性負相關。在 45 歲以上,這種關聯被認為具有統計學意義。
新研究的合著者Raphael Cuomo 解釋說:「我們在結直腸癌發病率中看到的大量差異是紫外線水平的差異造成的,尤其是對於 45 歲以上的人群。雖然這仍然是初步證據,但它可能尤其是老年人,可以通過糾正維生素 D 的缺乏來降低他們患結直腸癌的風險。」
2013 年的一項研究發現紫外線 暴露與結直腸癌之間存在類似的關系,這項新研究的結果與之前的研究結果一致。
在新研究中加入年齡相關評估表明,維生素 D 缺乏在主要是老年人的結直腸癌發病中起著更大的作用。研究人員假設這可能是由於慢性維生素 D 缺乏增加了一個人患結直腸癌的風險。
研究人員在報告中總結道:「這項研究支持制定適當的公共衛生計劃,以避免國家和全球層面的維生素D缺乏,無論是通過篩查高危人群、選擇性補充,還是通過食品強化等基於人群的措施。未來的研究可以旨在確定哪些癌症類型在補充維生素D後有明顯的改善。」
這項新研究發表在《BMC公共衛生》雜誌上。
來源:cnBeta
新證據表明維生素D的缺乏與患結腸直腸癌的的風險增加有關
基於長期以來將維生素D缺乏與結腸直腸癌風險增加聯系在一起的觀察,加州大學聖迭戈分校的一項新研究發現,在紫外線水平較低的國家,人們經常報告結腸直腸癌發病率較高。幾年來,研究人員已經檢測到低維生素D水平和結腸直腸癌之間的強烈關聯。然而,一些研究對這種聯系提出了質疑,發現幾乎沒有證據表明癌症和維生素D之間存在關系。
這項新研究採取了稍微不同的方法,研究了186個國家的全球紫外線暴露水平。研究人員考慮了幾個混雜因素,如皮膚色素和吸菸,同時也對年齡進行了調整。
該研究檢測到結腸直腸癌和紫外線照射之間存在明顯的年齡依賴性的反向關聯。在45歲以上,這種關聯被指出具有統計學意義。
新研究的共同作者Raphael Cuomo解釋說:「UVB光照的差異在我們看到的結腸直腸癌發病率的變化中占了很大一部分,特別是對於45歲以上的人。盡管這仍然是初步證據,但可能是老年人,特別是通過糾正維生素D的缺乏,可以減少他們患結腸直腸癌的風險。」
2013年的一項研究發現紫外線照射和結腸直腸癌之間有類似的關系,這項新研究的結果與之前的那些發現是一致的。
在新研究中加入年齡依賴性評估,表明維生素D缺乏在結腸直腸癌的發病中起著更大的作用,主要是在老年個體中。研究人員假設這可能是由於慢性維生素D缺乏增加了一個人的結直腸癌風險。
研究人員在論文中總結說:「這項研究支持有必要制定充分的公共衛生計劃,以避免國家和全球層面的維生素D不足,無論是通過篩查那些有風險的人,通過選擇性的補充,還是通過基於人口的措施,如食品強化。未來的研究可以旨在確定哪些癌症類型在補充維生素D後有明顯的改善。」
這項新研究發表在《BMC公共衛生》雜誌上。
來源:cnBeta
通過確定免疫療法誘發毒性的機制 科學家為減少副作用的癌症療法鋪平道路
通過確定免疫療法誘發毒性的機制,來自瑞士日內瓦大學(UNIGE)和哈佛醫學院的科學家正在為減少副作用的癌症治療鋪平道路。近年來,免疫療法已經徹底改變了癌症治療的領域。然而,健康組織中的炎症反應經常引發副作用,這些副作用可能很嚴重,並導致治療的永久中止。這種毒性仍然沒有得到很好的理解,是使用免疫療法的一個主要障礙。
來自日內瓦大學和哈佛大學醫學院的科學家們已經成功地確定了有害的免疫反應和那些針對腫瘤細胞的反應之間的區別,這些反應是人們所追求的。他們發現,雖然免疫機制相似,但涉及的細胞群卻不同。
這項發表在《科學免疫學》(Science Immunology)雜誌上的工作使研究人員有可能為癌症患者設想出更有針對性、更有效和更少危險的治療方法。
基於對病人免疫系統的大規模刺激,免疫療法已經拯救了許多生命。不幸的是,它們並非沒有後果。"當免疫系統被如此密集地激活時,由此產生的炎症反應可能會產生有害影響,有時會對健康組織造成重大損害,"UNIGE醫學院病理學和免疫學系及腫瘤血液學轉化研究中心的ISREC基金會腫瘤免疫學主席Mikaël Pittet說,他也是瑞士萊曼癌症中心的成員。
"因此,我們想知道,旨在消除癌症的理想免疫反應和可能影響健康組織的不需要的反應之間是否存在差異。識別這兩種免疫反應之間的獨特元素,確實可以開發出新的、更有效和毒性更小的治療方法"。
科學家們利用在CHUV和HUG接受治療的遭受這種毒性反應的病人的肝臟活檢樣本,研究了起作用的細胞和分子機制,以揭示相似性和不相似性。
類似的反應,但有不同的細胞
在免疫療法相關的毒性反應中,兩種類型的免疫細胞--巨噬細胞和中性粒細胞群--似乎負責攻擊健康組織,但不參與殺死癌細胞。相反,另一種細胞類型--樹突狀細胞群--不參與攻擊健康組織,但對消除癌細胞至關重要。
Mikaël Pittet解釋說:"免疫療法可以觸發專門蛋白質的產生,提醒免疫系統並引發炎症反應。在腫瘤中,這些蛋白質是受歡迎的,因為它們允許免疫系統摧毀癌細胞。然而,在健康組織中,這些同樣的蛋白質的存在可能導致健康細胞的破壞。因此,這些炎症蛋白在腫瘤和健康組織中由如此不同的細胞產生的事實是一個有趣的發現。"
樹突狀細胞非常罕見,而巨噬細胞和中性粒細胞則更為常見。一些巨噬細胞從胚胎發育階段就存在於我們的大多數器官中,並在我們的一生中一直存在。與以前的想法相反,這些巨噬細胞不一定能抑制炎症,但在免疫療法的刺激下,可以在它們所在的健康組織中引發有害的炎症反應,從而解釋了為什麼毒性會影響不同的器官。
當巨噬細胞被藥物激活時,它們會產生炎症性蛋白。這些反過來又激活了中性粒細胞,後者執行毒性反應。"Mikaël Pittet說:「這為通過操縱中性粒細胞限制免疫療法的副作用提供了可能性。」
科學家們通過研究小鼠的免疫反應證實了他們的發現,這些小鼠的細胞活性是用遺傳工具來調節的。他們能夠確定一個可以被利用來消除這些副作用的漏洞。事實上,中性粒細胞產生一些對毒性發展很重要的因素,包括TNF-α,這可能是一個治療目標。TNF-α抑制劑已經被用於調節關節炎患者的免疫反應,也許在癌症治療中也可以用來抑制免疫療法中中性粒細胞的毒性作用。
「此外,抑制中性粒細胞可能是一種更有效的抗癌方式:除了引發毒性反應外,其中一些細胞還促進腫瘤生長。因此,通過設法控制它們,我們可以產生雙重的有益效果:克服健康組織的毒性,並限制癌細胞的生長,」Mikaël Pittet總結道。
來源:cnBeta
這些色彩奇特的寵物壁虎 原來還藏著與人類癌症有關的秘密
豹紋守宮(Eublepharis macularius)是一種體型嬌小、長相可愛的壁虎,而且具有性情溫和、飼養難度低等優勢,成為爬行動物中最受歡迎的寵物。豹紋守宮最吸引愛好者的地方要數它們奇特的體色。豹紋守宮的原始體色類似豹子身上的黑斑,這也是它們得名的由來。
但在過去三四十年里,經過人工選育和繁殖,許多豹紋守宮的身上出現了絢麗的條帶和迷人的斑紋。根據色調的不同,有檸檬霜、蜜橘、黑夜、白騎士等各種名稱。
▲各種色彩的豹紋守宮,左上角的一隻是原色(圖片來源:參考資料;Credit: L. Guo et al. /PLOS Genetics 2021/Steve Sykes)
絢麗的豹紋守宮不僅吸引了爬寵玩家,還吸引了一些生物科學家。加州大學洛杉磯分校的Longhua Guo博士回憶說,當他在2017年剛剛進入遺傳學家Leonid Kruglyak教授的實驗室時,想要找一個有意思的課題。剛好,他在網上看到了一篇介紹豹紋守宮的文章。「我立馬被圖片吸引。」他說,「這些動物的顏色和圖案太奇特了!」
不過Kruglyak教授很清楚,要探索豹紋守宮體色背後的基因並非易事。盡管他的實驗室專長於揭秘不同生物各種性狀的遺傳基礎,但他從未研究過豹紋守宮。不像小鼠、斑馬魚等常見的實驗動物,其基因組序列早已被破解,有很多研究工具可以供科學家使用;對於蛇、蜥蜴等爬行動物,人們對其遺傳學的了解極為有限,連哪些基因位於哪條染色體上也鮮有人知。
受好奇心驅使的科學家們找到了一個合作者,當地一位狂熱的豹紋守宮繁育愛好者Steve Sykes先生。
說他狂熱一點也不夸張。Sykes先生飼養了數百條豹紋守宮。2015年,為了一見鍾情的一對豹紋守宮,Sykes先生曾經一擲千金,更確切的說,是1萬美元!
這一對豹紋守宮的顏色和Sykes先生過去見到的都不一樣,它們整個背部呈現漂亮的淡黃色,就像浸在了檸檬果凍里。這是一對剛剛繁育出的新品種,被稱作「檸檬霜」。Sykes先生給它們取名為霜先生和霜太太。
▲檸檬霜豹紋守宮,霜先生Mr. Frosty(圖片來源:參考資料;Credit:L. Guo et al./PLOS Genetics 2021/Steve Sykes)
Sykes先生向科學家們介紹了他的收藏。他有數量足夠多的豹紋守宮,更難能可貴的是,他還有詳細的繁殖記錄,這對於科學家們分析體色遺傳極有幫助。
Sykes先生也專門向Guo博士講述了「霜先生」的故事。在買下這對檸檬霜後,他讓霜先生和其他豹紋守宮進行雜交,希望生出更多漂亮的檸檬霜。然而,一年之後,他注意到了奇怪的事情:一些幼體的皮膚上長出了小小的白色腫塊。隨著時間推移,他發現,幾乎超過80%的檸檬霜個體會在出生後的五年里長出白色的皮膚腫塊。有些個體的腫塊會長得很大,導致動物行動困難;一旦破裂,還會引起感染。
因此,Sykes先生希望科學家們研究檸檬霜。他想知道,它們的皮膚腫塊和獨特的顏色是否有某種密不可分的聯系,是否有辦法讓培育出的檸檬霜避免這種命運。
▲80%的檸檬霜個體會長腫瘤(圖片來源:參考資料)
科學家們接受了建議。
他們從500隻豹紋守宮的尾巴或臉頰內側採集了DNA,包括霜先生的幾十個子孫,然後使用基因組測序技術閱讀它們的遺傳密碼。同時,根據每一隻的外觀和繁育記錄,研究人員可以確定它們有幾個檸檬霜等位基因。通過比較檸檬霜個體與原色個體的基因組差異,尋找基因組中檸檬霜個體與其他個體不同的片段。
研究人員最終破解了檸檬霜的遺傳密碼。他們發現,單個基因同時控制了顏色和癌症。通過各種基因分析,結果指向了基因組中的一個區域,該區域只包含一個已知的基因:SPINT1。
而這個SPINT1基因,已經被發現與癌症有關。該基因發生突變的人,更容易得黑色素瘤,一種致命的皮膚癌。鑒於這個基因在癌症中的已知作用,Kruglyak教授認為,他們找到了導致豹紋守宮長腫瘤的明確候選者。具體來說,檸檬霜個體擁有變異的SPINT1,該基因中的錯誤可能引起皮膚中的虹膜細胞(iridophores)過度增殖。
和熱帶魚、變色龍一樣,豹紋守宮的絢麗色彩來自虹膜細胞。虹膜細胞通過晶體產生顏色,這些晶體的形狀和結構會影響它們折射和反射光線的方式,從而產生各種顏色。豹紋守宮的虹膜細胞中,晶體排列產生白色。當虹膜細胞及其晶體過量產生,整體背景顯得更白,動物的黃色看起來更明亮,但也可能導致皮膚腫瘤的發展。
▲檸檬霜個體的皮膚腫瘤中,虹膜細胞內含有更多的反光晶體(左);相比之下,原色個體的皮膚中,虹膜細胞的密度較小,晶體較少(圖片來源:參考資料)
2021年7月24日,這項研究成果發表在學術期刊PLOS Genetics上。
得知這一結果,Sykes先生表示,他已經停止繁育檸檬霜個體,「我的目標是繁殖出美麗、完美、健康的豹紋守宮,而現在看來,似乎不可能將檸檬霜基因與腫瘤表型分離開來。」
而科學家們的研究沒有停止。最初只是出於對豹紋守宮奇特色彩的好奇,最終他們被帶到了一個出乎意料的方向。這項研究的發現,或許可以為研究人類黑色素瘤開辟新的途徑。例如SPINT1的突變究竟如何影響黑色素瘤的形成,仍然還是未解之謎,而虹膜細胞中的新發現,可能揭示重要的分子通路。
Kruglyak教授甚至期待,豹紋守宮或許還能成為爬行動物中的「小鼠」,作為未來研究癌症的新模型。
參考資料:
Longhua Guo et al., (2021) Genetics...
突破性的新血液測試Galleri可檢測出50多種類型的癌症
據媒體CNET報導,研究人員近日表示,一種名為Galleri的新血液測試能夠有效地發現50多種癌症,這些癌症在其早期階段往往沒有被發現。該測試為未來提供了一個充滿希望的前景,屆時新型的多種癌症篩查可以及早發現更多的癌症,從而挽救生命。
在美國,有幾種癌症篩查測試,但美國國家癌症研究所認為只有四種癌症的測試是有效的(結腸直腸癌、肺癌、乳腺癌和宮頸癌)。據Galleri的製造商Grail稱,被梅奧診所稱為 "突破性 "的多種癌症Galleri測試是為了補充現有的癌症篩查測試。
該測試在美國(除紐約州外的所有州)都有售,可由保健專業人員為50歲及以上的病人或有癌症風險的人訂購。但在Galleri被用作首選診斷工具之前,可能還需要幾年時間。
據生物制藥新聞網站Fierce Biotech報導,該測試還沒有得到美國食品和藥物管理局(FDA)的批准,Grail計劃在2023年尋求全面批准。而且還計劃對該測試進行更多的研究。據《衛報》報導,英格蘭公共衛生局將在今年秋天啟動Galleri的試點研究,預計在2023年獲得結果。
Grail公司在2021年的美國臨床腫瘤學會上展示了其自籌資金對Galleri進行研究的首批結果,其關於多種癌症測試的驗證研究數據周四發表在《腫瘤學年鑒》上,這是歐洲腫瘤醫學會的一份同行評審期刊。根據新研究,該血液檢驗在51.5%的病例中能正確地檢測出癌症,並且具有非常低的假陽性率。在檢測到癌症的情況下,該測試在88.7%的情況下可以確定它在身體的哪個部位。
據《衛報》報導,Galleri是利用一種識別模式的機器學習算法開發的。據Grail稱,該測試通過尋找血液中可能與癌症有關的信號來工作--特別是由腫瘤脫落的DNA,它可以顯示出異常的化學變化模式。在Grail的網站上,有一份Galleri可能檢測到的癌症的綜合清單。該公司的支持者包括科技名人傑夫·貝佐斯和比爾·蓋茨。
根據CDC的數據,2019年癌症是美國的第二大死因,最新Galleri研究的作者預測它很快將成為全球的主要死因。研究人員在研究報告中說,這種新的血液測試可用於檢測卵巢、胰腺、食道、胃、頭頸部和其他身體部位的癌症,這些癌症占美國癌症死亡人數的大約三分之二。
來源:cnBeta
研究人員希望mRNA疫苗也能幫助對抗癌症
由於不同領域的研究人員過去在mRNA疫苗技術方面投入了近20年的工作,今天世界各地的人們正在接受應對COVID-19的免疫接種以希望能帶領我們走出這種大流行病。現在,由於對這一多功能技術和這一研究基礎的進一步關注,用於其他疾病的mRNA疫苗有更大的機會讓人們受益。
佩雷爾曼醫學院傳染病研究助理教授諾伯特-帕爾迪說:"整個平台非常、非常靈活。你可以將mRNA疫苗用於許多方面"。這包括癌症--這只是賓夕法尼亞大學研究人員一直在研究的傳染病之外的幾個領域之一。
以下是關於基於mRNA的疫苗如何對抗腫瘤,需要克服的挑戰,該技術在腫瘤學中的根基,以及它的發展方向的詳細介紹。
保護與攻擊
疫苗用於治療癌症與用於治療像COVID-19這樣的傳染病的疫苗有一個關鍵區別。
首先,COVID-19的mRNA疫苗可以保護人們免受病毒侵害。它們是預防性的。但癌症mRNA疫苗是一種干預措施(一種治療方法),給予病人,希望他們的免疫系統能以攻擊腫瘤細胞的方式被激活。
通過他們的研究,帕爾迪和其他人包括開發BioNTech和Moderna疫苗的研究人員,佩雷爾曼醫學院傳染病學教授德魯·魏斯曼博士,以及賓夕法尼亞大學兼職副教授和BioNTech高級副總裁卡塔林·卡里科博士,發現mRNA疫苗不僅可以促使強烈的抗體反應來抵禦入侵者,如COVID-19,而且還能產生有效的細胞毒性T細胞反應。
這很重要,因為這些T細胞可以殺死癌細胞,它們只是需要被改變或被激勵來做這件事,這有點類似於免疫療法,如檢查點抑制劑或嵌合抗原受體(CAR)T細胞療法,它能使病人自己的T細胞找到並摧毀癌細胞。
帕爾迪說:"一個成功的治療性癌症疫苗應該誘導強烈的T細胞反應,特別是CD8+T細胞,它們具有殺死惡性細胞的已知能力,"他目前正在領導研究,以更好地了解治療癌症的mRNA疫苗,以及其他疾病。帕爾迪也是魏斯曼實驗室的一名博士後研究員,並且是他和卡里科的經常合作者。"治療性癌症疫苗將被給予癌症患者,希望這些疫苗誘導的細胞毒性T細胞能夠清除腫瘤細胞。"
一個例子是一種mRNA疫苗,它針對腫瘤上被稱為新抗原的蛋白質來對抗它。新抗原是當腫瘤DNA發生某些突變時在癌細胞上形成的一種新蛋白質。
必須克服個體差異問題
不過,開發這些類型的癌症mRNA疫苗的最大挑戰是它必須是多麼的個性化。每個人的大部分腫瘤新抗原對他們來說都是特定的。
它不能像其他疫苗一樣是一種包羅萬象的方法--它需要個性化,就像CAR-T細胞療法一樣,這需要採取病人自己的T細胞,設計它們來尋找腫瘤細胞上的特定抗原,然後將它們輸回體內以找到並殺死它們。
"這就是為什麼我們需要一種靈活而有效的疫苗技術,例如用於COVID-19的mRNA技術,"帕爾迪說。"它可以被開發出來,為我們提供個性化的新抗原疫苗。"
一種被稱為sipuleucel-T(Provenge)的類似的轉移性前列腺癌疫苗刺激了對前列腺酸性磷酸酶(或PAP)的免疫反應,PAP是存在於大多數前列腺癌上的抗原。雖然它不是mRNA技術,但它是為每個病人定製的,並且在臨床試驗中顯示,患有激素難治性轉移性前列腺癌的男性的生存率增加了約四個月。
到目前為止,它是唯一被美國食品和藥物管理局批準的疫苗。
mRNA和癌症護理、研究、學習和臨床試驗
引導我們開發COVID-19疫苗的不僅僅是多年的病毒學和免疫學研究。癌症研究也發揮了重要作用。
事實上,早在2008年,BioNTech的mRNA疫苗平台就首次被開發出來,並在人類中進行了實驗性的癌症疫苗測試,當時有13名黑色素瘤患者使用該mRNA平台進行了疫苗接種。
研究人員報告說,當他們被接種後,免疫系統對腫瘤的反應性確實變得高漲。因此,他們發生新的轉移性病變的風險明顯降低。Moderna公司的癌症mRNA疫苗採取了不同的方法,同樣誘發了實體瘤的免疫反應--這項工作也是在幾年前開始的。當他們將其與檢查點抑制劑相結合時,該療法使20名患者中有6人的腫瘤縮小。
"毫無疑問,今年在SARS-CoV-2疫苗方面所做的巨大的、前所未有的努力,是建立在我們的生物醫學界(包括癌症研究人員的關鍵貢獻)所做的強大的、長期的科學努力之上的。"系統藥理學和轉化治療學系主任、賓夕法尼亞州免疫學研究所所長John Wherry和他的合著者代表美國癌症研究協會的COVID-19和癌症工作組在《臨床癌症研究》雜誌的一篇文章中寫道。"如果沒有之前的這項工作,我們將非常落後於我們今天的水平。"
由BioNTech公司免疫受體療法主任Katharina Reinhard領導的一項更近期的臨床前研究也表明,當刺激和反應較弱時,RNA疫苗平台可以與CAR-T細胞療法結合使用以增強其效果。所謂的 "CARVac"方法激活了樹突狀細胞,這反過來又刺激和增強了CAR-T細胞的療效,研究人員去年在《科學》雜誌上報告了這一情況。
萊因哈德在賓夕法尼亞大學醫學院5月舉辦的 "21世紀細胞谷:細胞和基因療法的未來 "研討會上談到了這項工作。
雖然多年來出現的數據是有希望的,但只有少數研究報告了mRNA疫苗對癌症的臨床益處或免疫反應,而且沒有一個達到II期臨床試驗的水平。
因此,這項工作仍在繼續。而在去年,由於COVID-19的出現,這項工作才得以加速。
除了今天在學術機構進行的臨床前和臨床研究外,至少有八家制藥公司,其中許多與這些機構合作以研究癌症疫苗,包括研發新抗原的方法正在進行臨床試驗。
"多項癌症和傳染病mRNA疫苗臨床試驗正在進行中,未來幾年將是真正令人興奮的,並告訴我們更多關於mRNA疫苗的適用范圍,"帕爾迪說。
來源:cnBeta
研究發現白蘑菇中存在的化學物質或可減緩前列腺癌的進展
根據一項在2021年內分泌學會年會上公布的一項小鼠研究,白蘑菇中存在的化學物質可能減緩前列腺癌的進展。位於加州杜阿爾特的綜合癌症中心--希望之城醫學中心貝克曼研究所的首席研究員王曉強博士說:「雄激素是男性性激素的一種,它通過與雄激素受體結合並激活這種在前列腺細胞中表達的蛋白質而促進前列腺癌細胞的生長。"白金針菇似乎可以抑制雄性激素受體的活動。」
希望之城醫學中心貝克曼研究所的陳世安博士是這個項目的主要研究者,他以前對復發性前列腺癌患者進行了白蘑菇粉的一期臨床試驗,結果表明,白蘑菇降低了血液中的前列腺特異性抗原(PSA)水平,而且副作用很小。男性血液中PSA水平的升高可能表明前列腺腫瘤的存在。
這項新研究旨在了解這一發現背後的機制。研究人員研究了蘑菇提取物對對雄性激素敏感的前列腺癌細胞的影響。他們還研究了該提取物對植入人類前列腺腫瘤的小鼠的影響,這創造了一個動物模型,當研究被轉化為人類臨床試驗時,其結果將更加可靠。
研究人員發現,在前列腺癌細胞中,白蘑菇提取物抑制了雄性激素受體的活性。他們還發現,在用白蘑菇提取物治療六天的小鼠中,前列腺腫瘤的生長被明顯抑制,PSA的水平也下降。
「我們發現白蘑菇含有能夠阻斷小鼠模型中雄性激素受體活性的化學物質,表明這種真菌能夠降低PSA水平,」研究人員說。「雖然還需要更多的研究,但有朝一日白金針菇有可能為預防和治療前列腺癌作出貢獻。」
來源:cnBeta
研究發現前列腺癌跟肥胖存在關聯
據媒體報導,前列腺癌是加拿大男性中最常見的癌症,也是癌症死亡的第三大原因。腹部肥胖似乎跟患侵襲性前列腺癌的風險更大有關。這種聯系在Marie-Élise Parent教授領導的一項研究中得到了證實。相關研究報告已發表在《Cancer Causes & Control》上。
多年來,多項研究表明,肥胖是前列腺癌的主要風險因素。為了進一步探索疾病發病率和體重之間的聯系,研究小組研究了2005年至2012年在蒙特婁進行的一項調查的數據。研究人員發現,腹部肥胖跟患惡性癌症的風險增加有關。
Parent教授表示:「明確惡性癌症的風險因素是健康研究的一大進步,因為它是最難治療的。」另外她還補充稱:「通過更密切地監測有這一風險因素的男性,這些數據為預防工作創造了機會。」
腹部肥胖和普通肥胖
身體脂肪的實際分布似乎是這種疾病發展的一個重要因素:對一個人健康的影響取決於脂肪是集中在腹部還是分布在全身。這項研究的論文主要作者Éric Vallières指出:「腹部肥胖會導致激素和代謝變化,從而促進激素依賴性癌細胞的生長。腹部肥胖被認為跟睪丸激素的下降及跟惡性腫瘤發展有關的慢性炎症狀態有關。」
普通肥胖沒有顯示出跟腹部脂肪相同的相關性。這可能是由於檢測偏差和可能的生物學效應。「在肥胖人群中,用於早期檢測前列腺癌的蛋白質,前列腺特異性抗原(PSA),在血液中被稀釋,」Vallières先生說道,「這種血液稀釋使得癌症更難檢測。」
研究小組認為,應該優先研究一生中肥胖的發生時間,並對身體脂肪分布展開更深入的分析,進而可以為了解患前列腺癌的風險提供更大的幫助。
來源:cnBeta
研究發現使用他汀類藥物的心力衰竭患者的癌症風險降低
根據6月23日發表在《歐洲心臟雜誌》上的新研究,與非他汀類藥物使用者相比,在平均四年的隨訪期間,心力衰竭患者使用他汀類藥物與患癌症的風險降低16%有關。此外,該研究發現,使用他汀類藥物與同一時期死於癌症的風險降低26%有關。
以前的研究表明,心力衰竭患者患癌症的風險增加,可能是因為心力衰竭可能是通過炎症或遺傳因素等共同途徑致癌的。然而,對心衰患者使用他汀類藥物與患癌和死亡風險之間的關聯研究很少。目前對香港8.7萬多人的觀察性研究是調查這一問題的最大研究,作者認為他們的發現可以推及到其他人群。
該研究還發現,心力衰竭患者服用他汀類藥物的時間越長,他們患癌症的風險就越大。與使用三個月至兩年他汀類藥物的患者相比,在調整了可能影響結果的因素(如年齡、性別、吸菸、飲酒和其他健康問題)後,如果患者繼續服用他汀類藥物四年和六年,他們的風險降低了18%,如果他們服用六年或以上,風險降低了22%。
同樣,與服用3個月至2年的病人相比,如果患者保持服用他汀類藥物4至6年和6年或以上,死於癌症的風險分別減少33%和39%。
領導這項研究的香港大學的姚啟航博士說:「開始服用他汀類藥物十年後,心力衰竭患者死於癌症的比例為3.8%,非使用者為5.2%--死亡的絕對風險降低了1.4%。與那些只接受了三個月到兩年的他汀類藥物的人相比,服用他汀類藥物六年後患癌症的絕對風險降低了22%。」
在與來自新加坡國家心臟中心的Carolyn Lam教授和其他研究人員的合作下,姚啟航博士分析了香港87102名在2003年至2015年間因心力衰竭入院的患者的數據。患者被隨訪,直到他們被診斷為癌症、死亡或直到2018年底,以較早者為准。如果患者有癌症史或在首次診斷心力衰竭後90天內被診斷出或死於癌症,如果他們有愛滋病毒,或如果他們服用他汀類藥物少於90天,則被排除在研究之外。這樣就剩下36176名他汀類藥物使用者和50926名他汀類藥物非使用者進行分析。
在隨訪期間,共有3863名(4.4%)患者死於癌症,最常見的癌症類型是腸道、胃、肺、肝和膽道(肝臟)系統。
研究人員還發現,與非使用者相比,他汀類藥物使用者因任何原因導致的死亡都較低:十年時,60.5%(21,886人)的他汀類藥物使用者已經死亡,78.8%(40,130人)的非他汀類藥物使用者已經死亡,這意味著與非使用者相比,使用他汀類藥物與任何原因導致的死亡減少38%有關。
研究人員說,心力衰竭治療的進展,在1970年至2009年期間,五年生存率從29%提高到60%,但心力衰竭患者因其他原因,特別是癌症死亡的增加,抵消了這一進展。
姚啟航博士說:「心力衰竭是一種在全球范圍內不斷增長的疾病,由與心臟和血管無關的其他原因造成的死亡令人擔憂。我們的研究結果應該提高醫生對心力衰竭患者中癌症發病率上升的認識,並鼓勵他們對與心血管無關的結果給予額外關注。此外,我們的研究強調了心力衰竭和癌症發展之間的關系,並提供了有關在這些患者中使用他汀類藥物來減少癌症發病率和相關死亡的可能性的重要信息。」
「應該進行隨機試驗來進一步調查這個問題。此外,這些發現,結合以前的研究顯示心力衰竭和癌症之間的緊密聯系,呼籲採取潛在的策略來減少癌症的風險,如對心力衰竭患者進行癌症篩查。」
該研究的優勢包括其規模、使用來自全香港地區范圍的、經過良好驗證的電子醫療資料庫的數據,以及對可能影響結果的因素的調整,包括使用二甲雙胍和阿司匹林等已知可預防癌症的藥物。
這項研究的局限性包括:這是一項觀察性非隨機研究,這意味著它只能顯示他汀類藥物和較低的癌症風險之間的關聯,而不是說他汀類藥物導致了風險的降低;沒有關於可能影響癌症風險的因素的信息,如家族史;可能有其他可能影響研究結果的因素沒有包括在分析中;沒有關於心臟的左心室表現如何的信息,因此不可能評估使用他汀類藥物對左心室射血分數的潛在保護效果。
來源:cnBeta
研究發現攝入紅肉與結直腸癌發展之間的機制聯系
根據發表在美國癌症研究協會期刊《癌症發現》上的一項研究,表明DNA損傷的基因突變與紅肉的高攝入量和結直腸癌患者的癌症相關死亡率的增加有關。
哈佛醫學院醫學副教授、丹娜法伯癌症研究院的醫生Marios Giannakis博士說:「我們已經知道,食用加工肉類和紅肉是結直腸癌的一個風險因素。國際癌症研究機構在2015年宣布,加工肉是致癌的,紅肉可能對人類致癌。」
Giannakis解釋說,臨床前模型的實驗表明,食用紅肉可能會促進結腸中致癌化合物的形成,但尚未顯示出與患者結直腸癌發展的直接分子聯系。他說:「現在缺少的是證明病人的結腸直腸癌有特定的突變模式,可以歸因於紅肉。確定結腸細胞中可導致癌症的這些分子變化,不僅支持紅肉在結腸直腸癌發展中的作用,而且還將為癌症預防和治療提供新的途徑。」
為了確定與紅肉攝入有關的遺傳變化,Giannakis及其同事對900名結直腸癌患者的匹配的正常和結直腸腫瘤組織的DNA進行了測序,這些患者參加了三個全國性的前瞻性隊列研究之一,即護士健康研究和健康專家隨訪研究。所有病人在診斷出結腸直腸癌之前的幾年里都提供了關於他們的飲食、生活方式和其他因素的信息。
對DNA測序數據的分析顯示,在正常和癌症結腸組織中存在幾個突變特徵,包括一個指示烷基化的特徵,這是一種DNA損傷的形式。烷基化特徵與診斷前加工或未加工紅肉的攝入量有明顯關系,但與診斷前家禽或魚的攝入量或其他生活方式因素沒有關系。紅肉消費與本研究中發現的其他任何突變特徵都沒有關系。與之前將紅肉消費與遠端結腸的癌症發病率聯系起來的研究一致,Giannakis及其同事發現,遠端結腸的正常和癌症組織的烷基化損傷明顯高於近端結腸的組織。
利用一個預測模型,研究人員確定KRAS和PIK3CA基因是烷基化誘導突變的潛在目標。與這一預測一致,他們發現攜帶KRAS G12D、KRAS G13D或PIK3CA E545K驅動突變的結腸直腸腫瘤,與沒有這些突變的腫瘤相比,其烷基化特徵的富集程度更高。烷基化特徵還與患者的生存有關:與損傷水平較低的患者相比,腫瘤具有最高水平的烷基化損傷的患者的結直腸癌特異性死亡風險高出47%。
Giannakis說:「我們的研究首次確定了結腸細胞中的烷基化突變特徵,並將其與紅肉消費和癌症驅動突變聯系起來。這些發現表明,食用紅肉可能導致烷基化損傷,導致KRAS和PIK3CA的致癌突變,從而促進結直腸癌的發展。我們的數據進一步支持紅肉攝入是結腸直腸癌的一個風險因素,也為預防、檢測和治療這種疾病提供了機會。」
Giannakis解釋說,如果醫生能夠確定那些在遺傳上容易積累烷基化損傷的個體,就可以勸告這些人限制紅肉的攝入,作為一種精確的預防。此外,烷基化突變特徵可以作為一種生物標記物來識別患結腸直腸癌風險更大的病人,或在早期階段檢測癌症。由於它與病人的生存率有關,烷基化特徵也可能有潛力作為預後生物標志物。然而,Giannakis指出,未來的研究需要探索這些可能性。
該研究的一個局限性是研究參與者的潛在選擇偏差,因為在隊列研究中無法從所有發病的結直腸癌病例中獲取組織標本。Giannakis和他的同事目前的研究正在探索紅肉攝入和烷基化損傷在不同患者群體中的潛在作用。
來源:cnBeta
新研究展示如何在尿液樣本中檢測出腦瘤的生物標志物
據媒體New Atlas報導,雖然腦瘤可能通過頭痛、惡心或語言障礙等症狀顯示出來,但這些症狀往往在疾病晚期才出現。這使得早期診斷變得很棘手,盡管這樣做可以為患者帶來更好的結果。日本名古屋大學的科學家們已經展示了如何通過一個簡單的尿液檢測來實現這一目標,該檢測在早期實驗中顯示出很高的准確性。
當涉及到非侵入性和高效的癌症診斷時,尿液檢測與血液檢測一起,正在形成一種令人興奮的技術。通過掃描這些液體樣本中與疾病相關的生物標志物,科學家們已經展示了他們如何能夠在典型的臨床症狀出現之前很久就發現癌症。這些研究在涉及到膀胱、前列腺、胰腺甚至肺部的癌症時顯示出特別的前景。
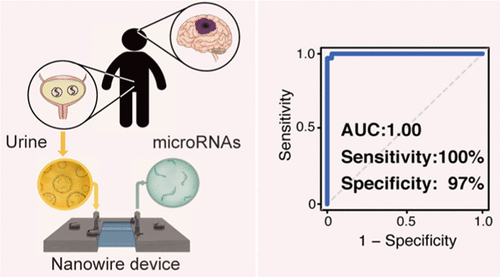
名古屋大學的研究小組試圖將這些可能性擴大到腦瘤,並得到了名為微RNA(microRNAs)的遺傳物質的幫助。這些是1993年首次發現的非編碼RNA的短鏈,在基因表達中發揮著重要作用,並且當由體內的癌細胞產生時可以採取獨特的形式。
科學家們試圖通過開發一種裝有1億根氧化鋅納米線的新型設備來利用這一點,該設備能夠從小至一毫升的尿液樣本中提取大量的微RNA。樣品從腦瘤患者和非癌症患者的對照組中收集,研究小組的分析顯示,許多來自腦瘤的微RNA可以在穩定狀態下的尿液中找到。
「基於尿液的液體活檢還沒有對腦瘤患者進行充分的研究,因為沒有一種常規方法能夠從尿液中有效地提取品種和數量方面的微RNA,」研究作者Atsushi Natsume教授解釋說。「因此,我們決定開發一種能夠做到這一點的設備。」
為了進一步探索他們的尿液檢測的潛力,科學家們分析了所收集的微RNA的表達譜,然後用這些來構建一個診斷模型。該模型隨後被用來區分腦癌患者和對照組,其靈敏度為100%,特異性為97%,而腫瘤的惡性程度和大小對結果沒有影響。
科學家們設想,隨著進一步的工作,這種類型的技術不僅可以為腦瘤的篩查提供有價值的工具,也可以為其他類型的癌症提供篩查。
Atsushi Natsume說:「在未來,通過人工智慧和遠程醫療的結合,人們將能夠知道癌症的存在,而醫生只需通過他們每天少量的尿液就能知道癌症患者的狀況。」
這項研究發表在《ACS應用材料與界面》雜誌上。
來源:cnBeta
研究人員將光敏藥物作為「特洛伊木馬」殺死癌細胞
據媒體報導,一種能夠進入並殺死細菌和癌細胞、而不傷害附近健康細胞的光活化藥物已經被成功測試。科學家們發現,將這種微小的殺滅細菌的分子與一種化學食物化合物相結合,可以誘使細菌攝取這種藥物。
這種分子--被稱為SeNBD--比現有的光敏治療方法更小,這意味著它可以更容易地穿過細胞的「防禦」。研究人員表示,需要進一步的測試來顯示該藥物是否是治療早期癌症和耐藥細菌的安全和快速方法。這項研究是在斑馬魚和人類細胞中進行的。
將藥物與代謝物耦合是關鍵
將藥物與食物化合物耦合是其成功的關鍵。細胞要生存,就必須消耗食物的化學成分--稱為代謝物--如糖和胺基酸,以獲得能量。
細菌和癌細胞很「貪婪」,傾向於攝入比健康細胞更高濃度和不同類型的代謝物。將SeNBD與一種代謝物配對,使其成為有害細胞的理想「獵物」。到目前為止,大多數光激活的藥物都比代謝物大,這意味著細菌和癌細胞不會把它們當作正常的食物來識別。
愛丁堡大學的研究人員發明了SeNBD,他們將其比作特洛伊木馬,並將其效果描述為代謝「彈頭」的效果。有害的細胞攝取了連結的藥物而沒有被提醒其毒性。
被可見光激活
除了足夠小以進入細胞外,SeNBD也是一種被稱為光敏劑的藥物,這意味著它只有在被可見光激活後才能殺死細胞。用光開啟藥物意味著外科醫生可以准確地決定他們希望藥物活躍的位置,避免攻擊健康組織的機會,並防止其他藥物造成的那種副作用。
首席研究員、愛丁堡大學轉化化學和生物醫學成像系主任Marc Vendrell教授說:
「這項研究代表了在設計新療法方面的一個重要進展,這些療法可以簡單地通過光照激活,一般來說非常安全。SeNBD是有史以來最小的光敏劑之一,它作為『特洛伊木馬』的使用為介入醫學開辟了許多新的機會,在不影響周圍健康組織的情況下殺死有害細胞。」
這項研究的結果發表在《自然通訊》雜誌上。
來源:cnBeta