健康長壽是每個人的希望,節食、輕斷食、生酮飲食、限時飲食等多種不同飲食策略改善健康的概念在公眾當中和科學界都引起了關注。這些飲食策略背後的科學基礎是什麼?近日,《科學》子刊Nature Reviews Molecular Cell Biology上的一篇綜述對不同飲食策略促進健康和長壽的機理進行了梳理。作者指出,理解這些飲食策略背後的分子機制,是基於這些機制,開發改善人類健康的飲食和藥物療法的關鍵。
▎藥明康德內容團隊編輯

節食與健康和壽命
過去幾十年里,在包括線蟲、果蠅、小鼠、非人靈長類動物在內的多種動物模型中,科學家們都發現,在維持營養供給的同時,降低熱量的攝入能夠延長動物的壽命。而且,這個延長壽命的效果包含兩個方面:1)節食能降低多種衰老相關疾病的風險,包括肥胖症、糖尿病、心血管疾病、癌症、炎症等等。2)節食還能影響動物的先天衰老過程,比如在實驗中節食的動物在生命的任何時期都比同年齡的非節食動物生理上更為年輕。
因此,科學家們也對節食激發的信號通路產生濃厚的興趣,希望從中找到節食改善健康的生物學基礎。
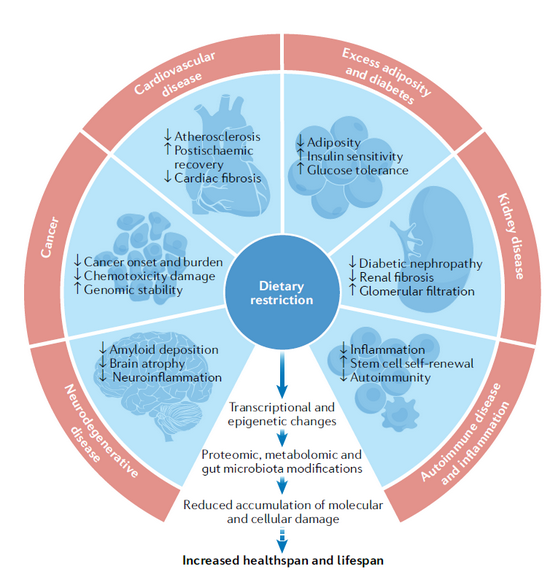
節食激發的信號通路變化
飲食限制通常會導致碳水化合物、蛋白質和脂肪攝入的減少,而科學家們已經發現這些營養物質水平的減少會在體內激發一系列信號通路的反應。比如,降低血液中葡萄糖水平和它的代謝產物會降低mTORC1信號通路,從而降低蛋白合成和增加自噬活動。而降低胺基酸水平對mTORC1有類似的影響。mTOR復合體是抗衰老領域大名鼎鼎的信號通路。
此外,降低蛋白和胺基酸水平會激發FGF21的表達,甲硫氨酸(Met)水平的降低會改變DNA和組蛋白的甲基化。
總體來說,節食會激發細胞的修復和回收利用途徑,包括自噬作用、線粒體自噬、DNA修復和氧化防禦,同時增強干細胞功能。結果是,細胞衰老(senescence)下降,蛋白質穩態得到改善。這些對細胞和組織的積極效果是延長生命和健康的因素之一。

不過對於大多數人來說,長時間的節食也太痛苦了!那麼基於對節食背後分子機制的了解,有沒有辦法在不節食的情況下獲得節食提供的好處呢?
特定食譜的效果
起初人們認為,節食帶來的好處是跟熱量攝入相關,不過近年來的研究發現,食譜的構成和攝入食物的時間在調節重要衰老信號通路方面也具有關鍵性的作用。
1。 蛋白限制食譜
在齧齒類動物模型中發現,限制飲食中的蛋白質會預防心血管代謝疾病和神經退行性疾病的風險,即使動物攝入的熱量總數沒有變化。而在人類中的大型流行病學資料庫顯示,攝入過多的蛋白質與肥胖、2型糖尿病和心血管死亡風險提高相關。
綜述作者指出,目前很多西方國家的成人每天吃的蛋白數量是建議蛋白數量的兩倍。過量的蛋白攝入導致體內胺基酸的水平升高,而胺基酸水平升高對前面提到的節食激發的信號通路產生相反的結果,包括mTOR復合體和FGF21的表達。
既然胺基酸水平在限制蛋白攝入的影響中起到重要作用,那麼抑制特定胺基酸的攝入能否達到同樣的效果?
2。 限制特定胺基酸的食譜
近年來,科學家們在檢驗限制特定的必需胺基酸水平,是不是可以獨立於總蛋白攝入和熱量攝入,延長健康壽命?潛在的候選胺基酸包括甲硫氨酸、支鏈胺基酸(branched chain amino acids,BCAA)等等。
甲硫氨酸在蛋白合成中處於一個獨特的位置,因為它對應的是蛋白合成的啟動密碼子AUG。因此,甲硫氨酸的限制會導致蛋白合成的顯著下調,這對健康衰老可能有益。
此外,甲硫氨酸水平的降低還能夠通過激活FGF21促進白脂肪組織的褐化,提高能量消耗。它還能改變DNA和組蛋白甲基化水平。在小鼠和大鼠模型中,降低甲硫氨酸攝入80%能夠將動物的壽命延長30%。
支鏈胺基酸包括亮氨酸、異亮氨酸和纈氨酸,血液中這些胺基酸水平的升高與肥胖和糖尿病相關。今年在自然子刊Nature Ageing上發表的兩項研究在小鼠和果蠅模型中也分別驗證了降低支鏈胺基酸攝入的好處。
相關閱讀:少吃這三種胺基酸,就能更長壽?兩項動物研究提示防衰老的飲食方法
從作用機制上來看,支鏈胺基酸是mTORC1的強力激活劑,因此食物中的支鏈胺基酸對於控制mTORC1的活性具有關鍵作用。
吃飯頻率和時間的影響
輕斷食的飲食策略通常指的是隔天,或者在一周中有不連續的兩天完全禁食或者攝入熱量很少。而限時飲食則將吃飯的時間限制在白天的某個時間段里。那麼,它們的科學基礎是什麼呢?
在小鼠模型中,間歇禁食(通常為24小時)可以激發某些長期節食激發的相同信號通路,包括降低氧化應激和炎症,增強自噬作用和組織修復能力,以及提高幹細胞功能。間歇禁食也能夠降低小鼠中很多慢性病的風險。
不過,綜述作者指出,小鼠的代謝速度和禁食能力與人類有很大的不同。小鼠的24小時禁食相當於人類的5天禁食。小鼠禁食導致的信號通路反應可能遠遠快於人類,因此不一定能夠將小鼠中的結果復制到人類中來。
而且,在間歇禁食實驗中,小鼠食用的是營養均衡的食物。而在現實中,很多禁食人群吃的食物並不健康,這可能導致維生素和礦物質缺乏,並且對代謝和腸道微生物組產生負面影響。
限時飲食的主要作用是將人體的生物鍾與因為飲食導致的代謝調節協調起來。已有的小鼠研究已經顯示擾亂生物鍾會導致肥胖、改變葡萄糖代謝並且降低動物壽命。在超重人群中進行的一些短期探索性試驗顯示,每天將吃飯時間段限制在8-12個小時內對體重和身體的肌肉組成產生有益影響。不過在大型臨床試驗中,這些益處尚未得到重復。
文章的最後,作者表示,對於如何將節食的益處轉化為臨床應用,我們仍然需要回答很多問題。未來10年的研究將專注於精細化理解食物中的組分(包括胺基酸、特定糖類、脂類以及微生物代謝產物)對健康生命的影響。值得注意的一個問題是人類具有遺傳學異質性,而遺傳和表觀遺傳背景也會影響對節食和其它飲食策略反應的效果。
作者期待科學發現迅速轉化成為將食物作為療法的個體化治療手段,能夠通過優化什麼時間,如何吃哪些食物,改善人類健康,延長人類生命。
參考資料:
[1] Green et al。, (2021)。 Molecular mechanisms of dietary restriction promoting health and longevity。 Nature Reviews Molecular Cell Biology, https://doi.org/10.1038/s41580-021-00411-4
來源:cnBeta