出品丨虎嗅科技組
作者丨馮丹丹
題圖丨IC photo
那一天,美國青年彼得帕克又想起了被蜘蛛支配的恐懼。
他被一隻受到核輻射的蜘蛛咬傷了手,不久之後,帕克發現自己居然擁有了「飛檐走壁」的超能力,背後的原因是他的基因與蜘蛛的基因進行了整合,漫畫家的腦洞瞄準了這一事物——基因(genetics)。

網友惡搞全球首例基因編輯嬰兒「締造者」賀建奎,其因觸犯非法行醫罪被依法追究刑事責任被判有期徒刑三年
腦洞先行,但人對探索基因的痴迷從未停止。類似「回歸子宮」這一心理現象,當自體向外發展至某一階段,我們總是逃不開向內探索生命意識本源的衝動,誰還沒個超級英雄夢呢?
同理,基因就是科學家的「向內」衝動。
2020 年,諾貝爾化學獎被兩名基因編輯領域的女性科學家(Jennifer Doudna 和 Emmanuelle Charpentier)捧得, 這項技術被稱為「CRISPR」,全稱為「Clustered Regularly Interspaced Short Palindromic Repeats」,它被浪漫化地比為「上帝的手術刀」。跳出電影和漫畫回歸現實,「上帝」能用CRISPR對基因「做手術」了。

兩位女科學家的獲獎海報
最近,圍繞CRISPR,Jennifer Doudna開發了一項新技術——不破壞DNA即能沉默基因。這一形容或許稍顯晦澀,但足以對人類個體產生影響。它是一段很長的故事,關乎生命,無法縮略。
你不是你,你是基因的合集
基因是什麼?高中生物課本中的大佬沃森和克里克告訴我們,基因是具有遺傳效應的 DNA 片段。DNA在動物體內呈現雙螺旋結構,由 A (腺嘌呤)、G (鳥嘌呤)、C (胞嘧啶) 和 T (胸腺嘧啶)這四種鹼基的排列組合組成,組合背後是密碼和奧義。
它決定了你的外在體徵,一定程度上影響智商、情商水平,更編排著疾病。你的一切由基因決定,生命的長度和厚度受其調控,這雙基因的「大手」在你的體內既能維持秩序又能翻雲覆雨。它干預著你的一切,除了靈魂,前提是如果靈魂真實存在的話。
編輯即為操作和改造,如文字編輯對字母的排兵布陣,基因編輯是對鹼基的再分配、添磚加瓦或斷舍離。添加想要的鹼基片段,切除累贅和病變的。
目標需要工具,上文提到的CRISPR即是目前最火熱的工具之一。自2002年在學生研究中被發現,2012年,在Jennifer Doudna 和 Emmanuelle Charpentier研究將原理成功破解,但仍未實現CRISPR的可工具化。直到2013年,諾獎有利的競爭者之一,華人科學家張鋒首次實現利用CRISPR編輯哺乳動物的基因,該成果在三大學術期刊之一 Cell 上發表,CRISPR正式俯瞰科學研究,舉步進軍產業。

基因編輯 SCI 論文數年度發展趨勢
從基因編輯出發,科學界開始向基因治療、疾病診斷進軍。2018年1月,美國宣布將在未來6年出資1.9億美元,支持體細胞基因編輯研究,以開發安全有效的基因編輯工具,治療更多人類疾病。
研究成果也不斷證實基因編輯在臨床治療中的美好前景,如治療杜氏肌營養不良(DMD)、帕金森(PD)、大皰性表皮鬆解疾病和α1-抗胰蛋白酶缺陷症、鐮刀型細胞貧血症、遺傳酪氨酸血症、白內障、先天性耳聾等。
看回國內,在精準醫療領域政策發布也非常密集,對基因編輯等技術給予大量支持。比如將精準醫療上升為國家戰略,計劃在2030年投入600億元。據中商產業研究院最新報告,2016至2020年全球精準醫療市場規模將以每年15%的速率增長。2020 年全球精準醫療市場規模將破千億,達到 1050 億美元,「基因剪刀」將是撬動千億級大市場的一把鑰匙。
它不完美
技術離完美永遠還差一步,CRISPR亦然,月之暗面在對DNA的破壞。
先看CRISPR/Cas9的原理圖。
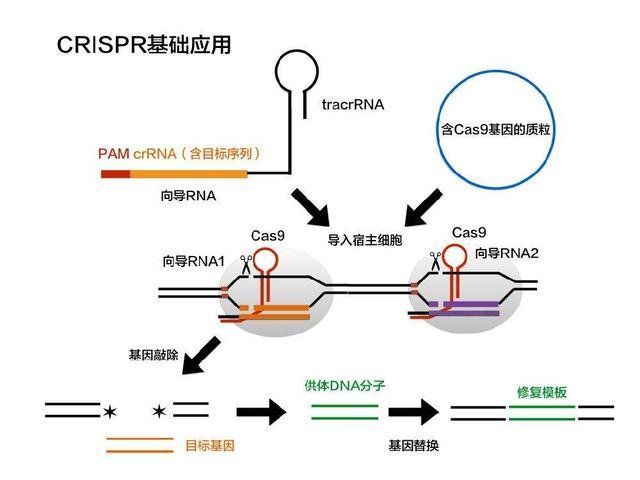
簡單理解,就是利用一個扮演GPS功能的RNA(sgRNA)識別目的基因,讓具備識別、切割功能的蛋白(Cas9)實現敲除、添加基因片段,以此達到及應變計的目的。不管是敲除還是插入,無一例外的,我們都需要首先讓DNA成功斷裂。不破壞就無法修改。
但科學家已經發現這背後的風險。sgRNA與Cas9蛋白這哥倆,並不是時時刻刻都兢兢業業工作的,誰還沒有倦怠的時候呢?本應該精準定位的sgRNA也有走眼的時候,本應該識別標準序列的Cas9蛋白,也偶爾不走心,結果就是「脫靶」,這將影響編輯的效率。
同時,基因編就可能引發的染色體破壞、致癌性、突變等問同樣觸目驚心。2019年,杭州市衛生健康委員會發布公告稱,2017年3月至2018年1月期間,時任杭州市腫瘤醫院院長的吳某帶領其團隊,對21名晚期食管鱗狀細胞癌患者進行了CRISPR基因編輯臨床試驗,導致杭州20名癌症患者死亡。
血淋淋的生命代價赫然在目,沒人願意為了傷敵一千連命都不要了。這讓文章最開始的研究擁有了用武之地。
疾病治療和新冠疫苗兩開花
先看Jennifer Doudna對這項技術的解釋,她將研究中利用的CRISPR工具命名為CRISPRoff和CRISPRon系統,主要用於誘導多能幹細胞轉化為神經元。Jennifer 團隊針對無解疾病阿爾茲海默症展開實驗,沉默了蛋白質Tau(目前的研究表明,蛋白質Tau是阿爾茲海默症主要病理表征之一)的基因。
Jennifer 認為,她們為傳統的CRISPR添加了一個開關(on-off switch)。

概念圖
「它改變了遊戲規則」,Jennifer 這樣形容,「更安全,對疾病的診斷和治療同樣有效」。原因在於她構建一種能夠模仿天然DNA甲基化的表觀遺傳編輯器,可以將甲基基團粘附在鏈上的特定位置,這些甲基化的基因就會被 「沉默」。 基因可以在DNA鏈的化學變化的基礎上被沉默或激活,而不需要任何劇烈和永久的變化。
簡單比喻一下。這個過程類似於「對鏡貼花黃」,你面部的瑕疵(致病基因)不用去掉,只要選擇一瓶合適的美妝產品(甲基基團)就能讓瑕疵被隱藏,粉飾的過程就是基因的「沉默」。
完美的隱藏和沉默是對上述20個生命的一次救贖,悲劇可能不會再重演。
Jennifer 本人給出結論稱,這種「升級版」的基因編輯技術為研究表觀遺傳機制、重大疾病治療以及研發新冠病毒疫苗等提供了有力工具。
最後,從生物技術行業的角度向下看去,技術更迭的進程組成道路。但略顯高調的看向人類世界,人生的點滴更加被技術左右。基因編輯,早不再屬於科幻,它就在你的身邊。
我是本文作者華北佛樓蜜,人類最後的嚴肅都該留給生物技術。珍惜所有與你溝通的機會,微信:Pinkfloyddddd,歡迎您來。
來源:kknews讓討厭的DNA「閉嘴」