隨著基因檢測和液體活檢等技術的進步,我們可以比以前更早地檢測腫瘤,但隨著而來的問題是我們能否預測癌症是否真正具有危險性?最近,《紐約客》(The New Yorker)的專欄作家悉達多•穆克吉(Siddhartha Mukherjee)博士的最新文章「癌症入侵的方程式」可能有助於我們瞭解關於癌症的最新觀點。通過跟許多腫瘤學研究專家進行交流,並且從一個生態入侵的故事中,穆克吉博士帶我們認識了癌症「土壤」和「種子」的觀點。穆克吉博士因為《眾病之王:癌症傳》獲得普利茲獎,他的另一部作品《基因:親密的歷史》被比爾·蓋茨先生推薦為2016年最佳書籍。
怪異的湖面
2011年夏天,密西根湖的水變得清澈透明。燈光斜照著湖面,像來自不明飛行物(U.F.O.)的探照燈;當你的視線穿透湖面,看見湖底的沉船一角,原本愉悅的感覺很快被恐慌所取代:一個自然界的湖泊看起來不應該像人造游泳池這般清澈見底!生物學家進一步調查後發現,通常湖泊里生長的上百萬浮游生物在這個湖中幾乎看不到,它們已經被一些貪婪的生物體吞噬。
罪魁禍首可能是某種軟體動物。1980年代末,從裏海和黑海駛來的貨船傾倒的水里攜帶了起源於烏克蘭河口盆地的物種——斑馬紋貽貝,從此對北美五大湖區造成了外來生物污染。
起初,軟體動物似乎是無傷大雅的客人。然後突然之間事情發生改變。1990年代中期,貽貝懸掛在沉船龍骨,渦輪機和螺旋槳上形成球莖和腫塊,覆蓋住碼頭,堵塞水管和衛生系統,並且沖刷岸邊,使得在一些湖灘上你幾乎是走在堅實的貝殼上。最終,水的清澈度開始增加,就像文中開頭的第一幕,可怕怪異。

▲密西根湖的湖岸線被斑馬紋貽貝占領(圖片來源:維基百科)
2012年底,密西根湖南部的貽貝密度竟然達到每平方米一萬個。而據估計,湖中有950萬億個貽貝,湖底部就像蓋裂痕的地毯。2015年,貽貝的密度達到每平方米一萬五千個,重量加起來比起湖中的所有魚類都重。過往船隻必須通過水清洗設備拆除和剝離貝殼,累計造成了數十億美元的損失。 「 不要移動貽貝!」 的雷達警告標誌被放置在湖泊中,而入侵者——斑馬紋貽貝的數目還在繼續蔓延。
為什麼貽貝會成為如此兇惡的入侵者?它們的一些侵略性是由生物學特徵決定的。斑馬貽貝是育種冠軍,每個個體每年可以產生超過一億個卵。然而,在烏克蘭河口盆地,這些貽貝很少達到北美五大湖區貽貝密度的五分之一。它們很少侵入30米以下的深度,堵塞船舶設備,或形成鈣質。簡而言之,它們是相對溫順的物種,也許是由水質、其天然的捕食者和病原體、流域的淺層或我們未知的因素限制了這些貝類的繁殖。

▲斑馬紋貽貝(圖片來源:維基百科)
解開這個奇怪謎題需要從兩個方面入手。一半的原因在於貽貝的內在生物學特徵——基因,形態,營養偏好,生殖習性。另一半涉及生物學與環境之間的相互作用。一個生態學本科生都能理解的概念是:生物體的「入侵」永遠是一個相對的概念。亞洲鯉魚是美國水域的另一個強大侵略者,但它們在亞洲並不具有侵害性。日本的蓼科雜草,現在殖民了英國的許多珍貴花園,但它們在日本幾乎不被稱為雜草。有時候,一個環境中的侵略者是另一個環境的良民。溫柔只是有條件的溫和,當條件改變時,它們可能會突然占領地球。
貽貝,蓼科雜草和癌症
六月份的一個晚上,當我走在芝加哥的密西根湖岸邊時,我想到了貽貝,蓼科雜草和癌症。當時上萬名專家抵達芝加哥,準備出席美國臨床腫瘤學會年會(ASCO),這是世界級的癌症大會。這個會議側重於討論癌細胞的固有特性,以及對抗癌細胞的治療方式。然而,這可能只是癌症認知的一部分。我們想知道正在對付什麼「軟體動物」,但我們也需要知道這是在哪個「湖泊」。
ASCO會議前幾週,我在哥倫比亞大學醫院(Columbia University』s hospital)遇到了一名乳腺癌女性患者。來自布魯克林的超市收銀員安娜·古澤洛女士(Anna Guzello)幾個月前就注意到了左乳房的小腫塊。之後,乳房X光檢查顯示出渾濁的,蜘蛛樣的腫塊,組織活檢證實是惡性腫瘤。
因為考慮到腫塊的大小和位置,簡單的腫瘤切除術不能防止復發,古澤洛女士接受了全面的乳房切除術,並計畫進行乳房重建手術。五月的一個下午,她拜訪了哥倫比亞大學乳腺腫瘤學家凱薩琳·克魯醫生(Katherine Crew),討論接下來的治療步驟。
克魯醫生告訴她:「首先,好消息。身體里沒有明顯的癌細胞。」

▲Katherine Crew教授(圖片來源:哥倫比亞大學)
外科醫生已經去除腫瘤,這是個好事。腋窩淋巴結(一個癌症經常轉移的部位)也沒有癌症的跡象。在腫瘤學上,古澤洛女士被歸類到NED(no evidence of disease):「沒有疾病的證據」。
但這只是一個毫無意義的短語:「證據」指的是我們的知識狀態,而不是疾病的狀態。乳腺癌細胞有可能離開了古澤洛女士的乳腺並且定居在她的大腦,脊髓或骨骼中,在那里它們可能處於掃瞄和測試不可見狀態。接受完全乳房切除術和「沒有疾病證據」的患者可能在切除原發性癌性腫塊幾個月,甚至幾十年後發生乳腺癌轉移性復發。癌症患者通常會死於這些轉移,而不是其原發性腫瘤(除了可以侵襲顱骨的腦癌,以及血液癌)。
「所以我們要繼續用藥物治療,以減少轉移的可能性,就是減少乳腺之外的地方會有癌細胞生長,」克魯醫生告訴古澤洛女士。她解釋說,這些藥物分為三大類:殺傷細胞的化療;靶向治療,如赫賽汀,特異性追蹤癌細胞中含有異常基因的產物;以及雌激素阻斷藥,通常要服用5到10年。
古澤洛女士摸了摸頭髮,嘴唇緊閉。激素藥聽起來很好,但是她對殺傷細胞的化療感到膽怯。
古澤洛女士說:「如果我沒有發生轉移,那麼我就是在無畏地冒險。」 這些風險包括:脫髮,腹瀉,感染,可能性很小的持續麻木(會讓她的手感覺像戴著皮手套一樣,對冷敏感)。化療意味著她需要到醫院輸液,每週一次,持續近半年。她家里還有一個嚴重殘疾的母親需要照顧,休假日也不多。有沒有辦法確定她發生轉移的可能性?「那樣我就可以更真實地評估治療風險和收益,」古澤洛女士說。

▲Daniel Hayes教授(圖片來源:密西根大學)
這個問題已經在腫瘤學領域迴響了數十年。直到現在,我們仍然不太擅長預測某個患者的癌症是否會轉移。密西根大學(University of Michigan)乳腺腫瘤學家丹尼爾·海斯博士(Daniel Hayes)在芝加哥的ASCO會議上告訴我,癌症轉移似乎像是隨機的暴力行為。「因為我們不能確定乳腺癌患者是否會有轉移,所以我們傾向於全部化療,好像每個患者都有潛在的轉移。」化療的毒性很大,化療的患者中只有部分人能從中獲益,但是我們不知道是哪一部分。所以,我們別無選擇,只能過度治療。對於像古澤洛女士這樣的女人來說,決策的難度不在於「為什麼是我」,而是「是否會是我」。
「種子和土壤」
一直以來,科學家認為癌症的轉移依賴於腫瘤棲息地。1889年,一名名叫史蒂芬·佩吉特(Stephen Paget)的英國醫生開始瞭解癌症的「生長及其次生長狀況」。他的父親James Paget是現代病理學創始人之一,叔叔是劍橋的醫學教授。在佩吉特時代,癌症被認為是從其原發部位擴散而成的惡性疾病,像滴在紙上的墨跡。外科醫生對這種癌症從中央不斷擴大的「離心理論」深信不疑,因此醫學界的主流觀點是通過外科手術徹底消除癌症(這個理論後來構成了外科醫生William Halsted推崇的乳房根治術的基礎。)

▲James Paget醫生是現代病理學創始人之一(圖片來源:維基百科)
但是當佩吉特醫生收集了死於乳腺癌的735名婦女的病例檔案時,他發現了一種奇特的癌症轉移模式。轉移似乎不是以離心擴散模式,而是離散地出現在腫瘤解剖部位遠處。而且傳播的模式也並非隨機:癌症對某些器官有著奇怪和強烈的偏好。在300多個轉移灶中,佩吉特醫生髮現241個在肝臟,17個在脾臟中,70個在肺部。
為什麼肝臟是轉移高發部位,而血液供應,大小和肝臟接近的脾臟卻不容易發生轉移?隨著佩吉特醫生的深入探索,他發現癌細胞甚至對同一器官中的特定部位也有偏好。骨骼是乳腺癌轉移的常見部位,但並不是所有骨骼都是同樣敏感的。「誰看過手骨或腳骨被二次癌症攻擊的?」
佩吉特醫生創造了「種子和土壤」一說來形容這一現象。「種子」是癌細胞,「土壤」是癌細胞繁殖的局部生態系統(器官)。佩吉特醫生的專注研究人體的癌症轉移模式。一個器官是否會發生癌細胞轉移似乎取決於器官的性質或位置——局部生態系統。然而,「種子和土壤」模式的邏輯最終引出了全局生態學的問題:為什麼一個人的身體容易受到影響,而另一個人卻不會?
佩吉特醫生提出的觀點——癌症轉移是癌細胞與其環境之間病理關係的結果,由於沒有確鑿的證據而被棄置了一個多世紀。直到1970年代,癌症轉移領域開創性的研究者以賽亞·費德勒博士(Isaiah J. Fidler)在美國國家癌症研究所(National Cancer Institute)工作時,開始研究組織與腫瘤之間的「對話」。費德勒博士提出,腫瘤是由數以百萬計的細胞的非均質混合物組成,只有一部分細胞離開原發腫瘤,與另一個器官的「土壤」形成聯盟,並引起轉移。

▲Isaiah J. Fidler博士(圖片來源:德州大學健康科學中心)
在同一時期,先在加州大學伯克利分校(University of California, Berkeley),然後在勞倫斯伯克利國家實驗室(Lawrence Berkeley National Laboratory)工作的米娜·比塞爾博士(Mina Bissell)開始研究腫瘤形成(或沒有形成)的微環境,找到能夠促進或阻止各種器官癌症生長的因素。她發現,環境至關重要。
癌症本位論仍占主導
然而,腫瘤學整體上仍然由簡單的模型主導。當我還是個醫學生時,曾經背誦過骨轉移癌症(乳腺癌,肺癌,甲狀腺癌,腎癌,攝護腺癌)的名單,當時我腦中出現了轉移瘤如何形成的畫面。癌症通過血管「傳播」,「攻擊」器官,並開始發芽和蓬勃生長。1990年代後期,我在在癌症病房輪轉實習時,那里的醫生強化了我這個想法。一名外科醫生曾在手術室對另一名外科醫生說道:「這個腫瘤侵襲了大腦。」 (相比之下,誰會說感冒侵襲了你)。這種說法包含主語,動詞,賓語:癌症是侵略者、轉移者。患者和他們的器官是受害者,被動的旁觀者。
這種語言模式反映了癌症本體論。即使研究範式轉移,這種思維仍然存在。麻省理工學院(M.I.T.)腫瘤生物學家羅伯特·溫伯格博士(Robert Weinberg)說:「癌症核心上是一種遺傳疾病」。因此,幾十年來,生物學家努力尋找使癌細胞異常生長,代謝,再生的基因突變。1980年代末期,以溫伯格博士為首的許多癌症生物學家致力於發現癌症轉移基因——met基因(藥明康德團隊註:指代metastasis)的作用。乳腺癌細胞有可能獲得一個突變,然後離開乳腺,到大腦里定居嗎?

▲Robert Weinberg博士(圖片來源:MIT)
儘管經過十多年的研究,met基因仍未找到。「我們從未找到任何東西,」溫伯格博士告訴我。有時在與原發性腫瘤不同的癌症轉移灶中檢測到突變,但突變不是轉移的單一驅動因素。
從1990年代末期開始,癌症遺傳學家嘗試了另一種思路。他們認為癌細胞中的突變不是孤立發生作用的,它們可以開啟和關閉其他幾十種甚至數百種基因。激活和抑制的這些基因可能會產生巨大的差異——就像同一個鍵盤可以發出截然不同的聲音,毛毛蟲和蝴蝶有相同的基因組但是長得完全不一樣,你的肝細胞與腦細胞也有相同的基因組但是它們功能不同。
這種從單個突變轉變為尋找基因調控模式——「基因表達標記」的方法,被證明是有效的。這種模式也被開發成預測性檢測項目,快速進入臨床。
在乳腺癌中,這種基因檢測已被廣泛使用,如MammaPrint和Oncotype DX,幫助醫生識別某些轉移性低風險的患者,並可以安全地避免化療。丹尼爾·海斯醫生說:「我們已經能夠在一些乳腺癌亞型中避免三分之一以上的患者過度化療」。
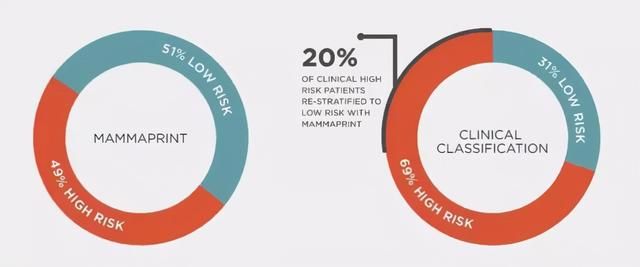
▲MammaPrint是一種預測乳腺癌復發率的基因檢測項目,數據顯示20%的患者通過該檢測重新定義為低風險,從而避免過度化療(圖片來源:agendia)
海斯博士認為基因檢測能使患者受益,例如高表達生長因子受體蛋白(HER2)陽性的乳腺癌患者建議服用靶向治療藥物赫賽汀,雌激素受體(ER)陽性的患者建議服用抗雌激素藥物。但是,儘管我們在使用遺傳標記物作為指標靶向腫瘤細胞方面取得了不少進展,但我們預測癌症轉移的努力進展緩慢。「是否會是我」這個問題依然困擾著整個腫瘤學領域。腫瘤學家哈囉德·伯斯坦博士(Harold Burstein)稱,化療的「不確定性盒子」仍然頑固地關閉。
腫瘤隨時都在釋放細胞
2001年,紐約紀念斯隆-凱特琳癌症中心(Memorial Sloan Kettering Cancer Center)的癌症生物學家瓊·馬薩圭博士(Joan Massagué)看到了一篇論文,徹底改變了他對轉移的想法。他花了幾年時間研究細胞生物學,闡明了乳腺細胞遷移到骨骼而不是大腦的基因調控機制。然後在一本晦澀的雜誌上一篇30年前發表的文章里,他找到了一個關鍵證據。這篇文章中寫道,美國國立衛生研究院(National Institutes of Health)的研究人員將乳腺癌細胞植入雌性大鼠的卵巢,細胞生長形成豆粒腫瘤。然後,研究人員每隔幾個小時從靜脈中抽出血液,計算腫瘤脫落的癌細胞數目。

▲Joan Massagué博士(圖片來源:紀念斯隆凱特琳癌症中心)
結果令調查人員感到困惑。他們發現,大約每24小時,每毫升血液里有兩萬個癌細胞。按照大約三百萬個癌細胞1克來估算,在一天之內,腫瘤的重量減少了近十分之一。後來科學家採用更複雜的方法和動物腫瘤進行了更多研究,證實腫瘤不斷地向外釋放細胞!(雖然局部的人體腫瘤釋放率較難研究,但現有研究結果已經證實了這個一般現象)
「我們認為轉移是一個持續的現象,」馬薩圭博士說:「我們需要找到允許細胞脫離腫瘤並進入血液和淋巴結的物質。如果原發性腫瘤持續地分泌細胞,並且每個細胞都能夠形成轉移,那麼患者的身體里應該存在無數可見的轉移性腫瘤。如果是這樣,古澤洛女士女士的乳腺腫瘤會轉移到大腦,骨骼和肝臟中。可是為什麼她的身體的其他地方沒有明顯的疾病證據呢?真正的難題不是為什麼某些癌症患者會發生轉移,而是為什麼不是所有癌症患者都發生轉移。
馬薩圭博士說:「轉移不足的唯一合理解釋是細胞大量死亡或細胞休眠浪潮限制了轉移。腫瘤脫落的細胞要麼被(免疫系統)殺死,要麼停止分裂進入休眠。當腫瘤細胞進入循環系統時,它們會立即發生大規模滅亡。只有少數癌細胞能夠到達目標器官,如大腦或骨骼。」在那里,它們面臨著在陌生和敵對環境中生存的難題。馬薩圭博士推斷,那幾個倖存的細胞必須處於休眠狀態。「只有當休眠的癌細胞重新激活並開始分裂後,才會發生臨床上可見的轉移——用CT掃瞄或核磁共振檢測的轉移病灶。」
惡性,不僅是指癌細胞的擴散,也包括停留和繁殖。
韓國的甲狀腺癌早期篩查
2012年春天,馬薩圭博士等人正在尋找休眠癌細胞,但達特茅斯學院(Dartmouth College)流行病學家吉爾伯特·韋爾奇博士(Gilbert Welch)則專注於另一個不同的問題:癌症早期發現。早期檢測旨在捕獲和消除癌症,避免轉移,但是一些癌症篩查項目的死亡率統計研究數據並沒有顯示出篩查的益處。

▲Gilbert Welch博士(圖片來源:達特茅斯學院)
韋爾奇博士告訴我一個流行病的故事。在大約15年前,韓國開始進行甲狀腺癌篩查。首爾的初級保健辦公室配備了小型超聲波設備,試圖發現最早的癌症徵兆。當發現一個可疑的結節時,就會進行活檢。如果病理報告為陽性,就採取甲狀腺手術切除。
甲狀腺癌的官方發病率——特別是稱為甲狀腺乳頭狀癌的亞型——在韓國範圍內開始飆升。2014年,甲狀腺癌發病率達到1993年的15倍,成為該國最常見的癌症。用一位研究員的話,好像一場「甲狀腺海嘯」突然襲來。數十億韓元花費在治療上,成千上萬的甲狀腺被手術切除。然而人們死於甲狀腺癌的比例卻保持不變。
究竟發生了什麼?這不是醫學上的錯誤:在顯微鏡下觀察到有問題的結節的確符合甲狀腺癌的標準。然而,病理學家發現的這些甲狀腺癌幾乎沒有引起疾病的傾向。患者沒有被誤診但被過度診斷;也就是說,這些切除的是可能永遠不會產生臨床症狀的腫瘤。
許多不同腫瘤類型的研究都佐證了這個觀點。1985年,芬蘭的病理學家對101名死於不相關的事故(車禍或心臟病發作)的人進行屍體解剖,以確定他們是否有甲狀腺乳頭狀癌。令人驚訝的是,三分之一的腺體中都有甲狀腺癌。另一個乳腺癌的類似研究比較了屍體解剖中可檢測的乳腺癌與終生乳腺癌死亡風險的關聯,結果表明過激的早期檢測可能造成乳腺癌過度診斷頻率激增,導致不必要的干預措施。調查了攝護腺癌篩查結果後,韋爾奇博士計算出,30到100位男性都經歷了不必要的治療,通常是外科手術或放射治療。
海斯醫生告訴我:「通過乳腺X線照相術早期發現乳腺癌可以拯救婦女的生命,雖然益處很小」。但同樣重要的是我們要如何處理檢測到的腫瘤:我們可以分辨出哪些腫瘤需要用化療或其他幹預措施進行系統治療嗎?海斯醫生繼續說道:「我們想要實現的不僅僅是早期檢測,而是早期預測」。
對於韋爾奇博士來說,診斷為甲狀腺癌或攝護腺癌的病例飆升,但是對總體死亡率沒有影響,這是一個警告:一知半解是一件危險的事情。癌症篩查運動擴大了疾病發現率,但是卻不能告訴我們在某種特定情況下是否需要治療。早期檢測幫助我們判斷「何時」和「什麼」,但沒有告訴我們「是否」。還有一個神秘的元素是,為什麼一些癌症擴散會致死,但仍有許多癌症是溫和的?
2012年3月的一天,韋爾奇博士飛往華盛頓參加了一個關於癌症轉移的會議。一張幻燈片引起了他的注意,它描繪了密西根湖的貽貝侵略。演講者肯尼斯·皮塔博士(Kenneth Pienta)是密西根大學(University of Michigan)的腫瘤學家,他聽說過貽貝危機,並且發現這與癌症很相似。研究人員不再將侵襲性視為癌症內在本質,而是癌症與環境之間的病理關係。
「癌細胞和宿主細胞形成了一個生態系統。最初,癌細胞是新環境的入侵物種。最終,癌細胞與宿主細胞之間的相互作用創造了一個新的環境。不僅要問癌症對你做了什麼,也要關心你對癌症做了什麼」。

▲Kenneth Pienta博士(圖片來源:密西根大學)
皮塔博士繼承了佩吉特醫生和費德勒博士的傳統,更加重視癌症發生的「土壤」。一名原發性乳腺癌的患者其實陷入的是一場沉默的戰爭。幾代腫瘤學家的研究試圖找到這場拉鋸戰的一個可能結果:當患者失利,她就死於轉移。但是當癌症失利時會發生什麼?也許癌細胞曾試圖入侵新的部位,但由於免疫系統和其他生理挑戰而在途中被消滅;也許最終有那麼幾個細胞經過遠征後倖存,到達新器官,它們像種子落在鹽灘上。
韓國的甲狀腺癌篩查的故事,讓流行病學家韋爾奇博士陷入了迷惑。我們必須警惕猖獗的斑馬貽貝和瀕危的紫貓爪貽貝之間的差異——但是北美區五大湖與狄更斯湖之間的區別呢?有證據表明,大多數患有攝護腺癌的男性將終生都不會發生轉移。是什麼使其他人更容易受癌症傷害?韋爾奇博士知道,通常的方法是在癌細胞中尋找標記物,以找到基因激活的模式,其中某些模式會導致癌症的危險性。這些尋找癌細胞的特徵的方法顯而易見是解決問題的關鍵。
但是,皮塔博士認為這種做法太狹窄了。對抗癌症的部分答案可能在於癌症與其宿主之間的「種子與土壤」的生態關係。
兩個澳大利亞黑色素瘤患者的故事
1992年,一位50多歲的澳大利亞高中老師被診斷患有黑素瘤,他左腋到身體都出現黑色條紋。診斷後的幾週,腫瘤的邊界開始發生變化。一邊變灰,另一邊縮小。「他出現一個經典的自發性消退,通常是癌變病變是被免疫系統控制的標準,」患者的兒子大衛·亞當斯先生(David Adams)告訴我。手術切除原發性黑色素瘤後,一直沒有發生轉移。但他父親有一個50多歲的朋友就沒有那麼幸運:他的原發性黑色素瘤被發現時,大腦里已經出現可見的轉移灶。

▲David Adams博士(圖片來源:桑格研究所)
亞當斯博士在雪梨學習遺傳和生理學,後來加入劍橋的桑格研究所(Sanger Institute),領導一個研究黑色素瘤生物學的小組。他沒有忘記他父親的案例,這是驅使他從事科研的原因。是什麼使黑素瘤在一個人體內消退,但是在另一個人體內進攻?
偶然地,亞當斯博士在關於腎臟捐獻的醫學文獻報導中得知一個黑色素瘤病例。一個患者——簡稱他為DG——被診斷患有黑色素瘤,並且經過手術成功切除。幾年後,被認為是完全健康的DG向朋友捐獻了一個腎。朋友服用了常規的免疫抑制劑,以防止腎臟抑制排斥。然而,幾個星期後,接受者的腎臟中幾百個黑色素瘤開始發芽。這些奇怪的黑素瘤來自DG的細胞。捐獻的腎臟必須馬上被切除。但是這時候,捐獻者仍然保持健康,他的體內並沒有黑色素瘤的跡象。
亞當斯博士認識到,原始宿主環境在限制轉移性增生方面發揮了至關重要的作用。捐獻者的黑素瘤細胞在他的腎臟中處於休眠狀態,類似於馬薩圭博士在小鼠中發現的休眠現象。當休眠的細胞到達免疫抑制的受體中時,「土壤」改變,癌症開始生長。亞當斯博士告訴我:「捐獻者的免疫反應肯定限制了轉移性癌症的發展」 。
2013年,亞當斯博士開始計畫一個雄心勃勃的實驗來確定癌症抑制宿主因素。他打算利用一個含有數百種遺傳改變的小鼠樣本庫,將相同的癌細胞植入這些樣本,研究哪些樣本會允許癌症轉移,哪些會抑制轉移?
這是一個巧妙的顛覆經典的實驗策略。幾十年來,生物學家一直在改變癌細胞的基因,並將細胞注射到幾個標準化的小鼠中。「不同癌症進入同一樣本」實驗允許癌症生物學家觀察癌症基因的變化如何影響其生長,代謝和轉移。但宿主基因組的變異會有什麼影響?亞當斯博士的「同樣的癌症進入不同樣本」實驗將注意力從「種子」轉移到「土壤」。
雞翅膀的實驗,以及三個小鼠實驗
1980年代,比塞爾博士曾經做過的一個迷人的實驗。當在雞的翅膀里注射致癌病毒,那里會生成腫瘤。如果注射一個翅膀,並且弄傷另一個翅膀,則受傷翅膀也會生長腫瘤。但是,如果向小雞胚胎注射致癌病毒,就不會發生腫瘤。比賽爾說:「那時候,人們只是把癌症看作致癌基因(oncogene)驅動的反應。但是現在看來,致癌基因也需要通過局部環境開啟或關閉」。
雖然種子很重要,土壤的特徵也可能影響它是否會發芽。
在紐約和波士頓,馬薩圭博士和溫伯格博士等研究人員也在調查「宿主因素」。溫伯格博士和他的同事們研究了一組老鼠,它們的肺部已噴灑數千個休眠的癌細胞。一些小鼠被暴露於炎症刺激,它們體內的癌細胞甦醒並變得具有侵襲性。
馬薩圭博士和他的學生進行了一項特別的實驗,他們在攜帶休眠癌細胞的小鼠中去除各種免疫細胞。某些免疫細胞類型屬於「獲得性免疫」系統,其中包含T細胞和B細胞,這兩種免疫細胞能夠識別並且記憶新的病原體,並在它們下一次出現時將其捕獲。獲得性免疫是疫苗的原理基礎,這也是為什麼人們很少會兩次得水痘。
但是在馬薩圭博士的試驗中,最令人吃驚的效果發生在另一種類型的免疫細胞——自然殺傷細胞(NK細胞)上。這些細胞屬於我們的「天然免疫」系統 ——它們的能力不是學習並識別任何新的病原體,而是被預先編程好隨時消滅病態或異常的宿主細胞。馬薩圭博士的團隊認為,NK細胞是癌症轉移的關鍵控制者。
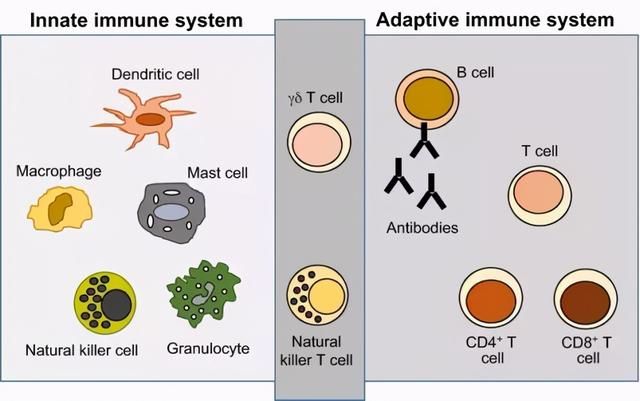
▲天然免疫(左)和獲得性免疫(右)系統的細胞類型(圖片來源:dmm.biologists.org)
與馬薩圭博士團隊關注的細胞類型不同,亞當斯博士感興趣的是宿主基因可能影響癌症轉移。2013年初,亞當斯博士實驗室的博士後,恰好也是他妻子的路易斯·范德韋恩博士(Louise van der Weyden)把一種小鼠黑色素瘤細胞(一種咖啡黑色漿液)的懸浮液注射到數十幾隻小鼠品系中。幾個星期後,她計算了每隻小鼠肺部可見的轉移灶數量,拿到數據的第一時間衝進亞當斯博士的辦公室。
亞當斯博士回憶說,即使在這麼小的研究隊列中(十幾隻小鼠),結果的差異也是顯而易見的。一些小鼠發生了數百個轉移,形成一連串黑色斑點。轉移最嚴重的小鼠的肺部明顯變黑。然而,有些老鼠幾乎沒有轉移。亞當斯博士說:「這證明了同一種癌症在不同的宿主環境中可以發揮如此不同的效果。」
兩年後,范德韋恩博士累積接種了810隻黑色素瘤小鼠,並分別檢測了癌症轉移病理特徵。結果發現,有15種小鼠顯示出對癌症轉移的中度或高度抗性。這15個小鼠品系中的12個含有影響免疫調節的基因變異,再次表明基因突變在癌症傳播和侵襲能力中的有力作用。其中有一隻小鼠表現尤為突出。暴露於研究中使用的癌細胞劑量時,正常小鼠大約發生250個轉移病灶。然而,這種抗性小鼠平均只有15到20個轉移灶。其中有幾隻老鼠一點都沒有轉移,暴露兩個月後,它們的肺部看起來完好如初。
為了確定這種抗轉移特性是否只限於黑色素瘤(一種公認能引起免疫反應的癌症類型),亞當斯博士和范德韋恩博士測試了另外三種類型的癌症:肺癌,乳腺癌和結腸癌。在所有這些癌症中,這種抗性小鼠都缺乏癌症轉移。進一步研究發現,該小鼠中稱為Spns2的基因發生變異,通過一系列級聯反應,增加了肺部免疫細胞,特別是NK細胞的濃度——這恰好是馬薩圭博士實驗室發現的具有最強的限制癌症轉移能力的免疫細胞類型!
亞當斯博士的父親的黑色素瘤從他50多歲確診後一直沒有復發,他最後死於攝護腺癌。亞當斯博士說:「幾年前,我可能會考慮這是黑色素瘤與攝護腺癌本身轉移潛力方面的差異。它們是『壞』癌症與『好』癌症的代表。但現在我會更多的思考:為什麼我父親的體內更容易發生攝護腺癌轉移,而不是黑素瘤轉移?」
「土壤」療法的興起
這種既考慮種子,也考慮土壤的方式,會得到重要的發現。像貽貝一樣,癌症在適合的棲息地中增殖,它們可以改造微環境,幫助它們抵抗敵人。「種子」療法殺死細胞——就像往湖里噴灑毒藥消滅貽貝。而「土壤」療法改變棲息地。
最近在癌症治療中最成功的創新之一是免疫治療,激活患者自身的免疫系統去攻擊癌細胞。多年前,先驅免疫學家吉姆·艾里森博士(Jim Allison)和他的同事就發現,癌細胞通過特殊的蛋白質來對宿主免疫細胞的功能進行抑制,使自己不受限制的生長。用進化的語言描述就是:能夠阻斷宿主免疫攻擊的癌細胞克隆具有自然選擇和生長優勢。
當Allison博士和他的同事用某些藥物阻止癌症的剎車蛋白起作用時,免疫細胞就開始對癌症發動進攻。據此,他發明了第一個免疫治療藥物Yervoy,2011年獲批上市治療惡性皮膚癌。這種變革性的免疫療法藥物也被稱為檢查點抑制劑(checkpoint inhibitors),被認為是化療之後腫瘤治療歷史上的最重要突破。藥明康德微信公眾號對此曾做相關報導。

免疫療法先鋒James Allison博士與他最初的夢想
免疫療法就是一種「土壤」療法。它不直接殺死腫瘤細胞,或者靶向腫瘤細胞內的基因突變產生的蛋白,而是在組織微環境的免疫上起作用,並改變宿主的生態。但「土壤」療法不僅是免疫因素,必須考慮到各種各樣的組織環境特徵。與癌症相互作用的細胞外基質,供給腫瘤細胞生長營養的血管,宿主的結締組織細胞的性質——所有這些因素都會影響組織的生態,從而影響癌症的生長。
亞當斯博士正在進行一項具有潛力的臨床研究,利用原發性黑素瘤的患者(像他的父親一樣)捐獻的血液,研究其中的遺傳標記物和免疫細胞組成。目的是通過長期跟蹤研究,我們可能發現對癌症特別敏感或抵抗的患者群體,從而更好地瞭解哪些患者需要積極治療。我們還可能學會如何治療癌症——改變易感患者的免疫學和組織學特徵,使他們體內環境特徵變得跟抗性人群類似。
應該關注分子還是分母?
1962年,英國醫生和癌症研究員史密瑟斯博士(DW Smithers)在《柳葉刀》中寫道:「癌症不是汽車故障,而是一種交通堵塞」。交通堵塞的原因是汽車和環境的關係發生問題,因此無論汽車本身能否正常運行都可能發生。史密瑟斯博士的觀點超越了時代,因此並沒有得到認同。在他死後,才人們才開始逐漸領悟他傳遞的信息。
想像有一天早上你坐地鐵時,旁邊一個戴帽子的男士打了一個噴嚏。在那個星期里,你感冒了。你可能是被那名男士傳染了。但你沒有想到的是,坐在他旁邊的另外六名乘客也受到那個噴嚏的影響,不過他們都沒有生病。
這是醫學上的「分母問題」。分子是生病的人,你。分母是每個處於風險中的人,包括所有其他暴露的乘客。分子容易研究,分母卻很難。分子來到醫院,抽血檢查開藥;分母從地鐵站回家,吃晚餐看電視。分子存在,分母消失。
為什麼分母不生病?因為病原體暴露相同,宿主卻不同。然而,「病原體」這個術語也有誤導性。病原體的定義是它具有致病性。但致病性不是固有的屬性,而是一種與宿主的互動關係。耶魯大學(Yale University)免疫生物學家盧斯蘭·梅德澤托夫博士(Ruslan Medzhitov)長期研究宿主和病原體的相互作用。他說:「將相同的病毒注入不同的宿主,會得到截然不同的響應」。宿主是決定疾病性質的土壤。
如果回到癌症早期檢測的問題。假設我們可以在人體內安裝微小的傳感器,定期掃瞄血液中的循環腫瘤細胞,進行持續的「液體活檢」。那我們可以更早地捕捉到癌症信號。但是,和首爾的醫生一樣,最終也可能只是比以前過度治療了更多的患者。因為循環腫瘤細胞可能會預測一些患者體記憶體在轉移性癌症,而在其他患者中,轉移並不會真正發生。為什麼沒有發生轉移?老的答案是:癌症是錯誤的客體。而新的問題是:我們應該尋找正確的主體嗎?
幾個月前,一名四十多歲的女士來到我的辦公室,顯得非常恐慌。她曾經因為子宮內膜異位症接受子宮切除術。在術後檢查子宮時,醫生髮現她還有一種罕見的,惡性的肉瘤。由於肉瘤太小,以至於無法在任何術前的掃瞄中看到。她曾先後諮詢了婦科和外科醫生,他們都建議採取侵略性手術切除卵巢和周圍的組織,這是一種根治的手術,會造成許多長期的副作用。但是醫生的理由是,一旦腫瘤擴散,就沒有辦法治療了。大多數診斷為這種肉瘤的患者,僅能存活兩三年。
但我認為這名女士的情況有些不同。她是在偶然情況下發現腫瘤,並沒有癌症的症狀或體徵。如果我們對一萬名無症狀的女性抽檢,不知道會隨機發現多少例這樣的惡性病變。而且我們並不知道,這些偶然發現的腫瘤對實際生活會有何影響。這個女士的腫瘤細胞和組織細胞之間的關係會導致癌細胞廣泛轉移擴散?還是會自然地抑制腫瘤的生長並阻止其擴散?沒人可以判斷。
但我的回答似乎令人非常不滿。她看著我,好像我瘋了。她質問道:「請問如果你身上發現了這個腫瘤,你能坐視不理嗎?」最後,她還是決定進行手術。
即使以傷害身體為代價,我們也會傾向於規避風險,因為我們不知道如果不做任何治療會發生什麼。
乳腺癌患者古澤洛女士則做了相反的決定。她同意服用雌激素抑制劑他莫昔芬。但她拒絕化療和赫賽汀,儘管檢測結果顯示HER2陽性。不過,克魯醫生醫生對她未來的預後情況也無法打包票。
「分母」是符合診斷測試標準,患有疾病的風險,但可能沒有實際患病的人。幾十年來,我們對「分母」的解釋標準一直很隨機,生病像是擲骰子的結果。但是為什麼許多暴露於疾病風險的人最終不會得病。梅德澤托夫博士提出了一個「組織參與新規則」的理論認為,我們所有的組織都具有「細胞之間互動和聯盟的規則」。生理學是這些關係的產物。
如果進一步考慮我們體內的「分母」問題。人體內有幾十萬個細胞;其中大部分都不一樣,而且幾乎總是不完美。即使在完全健康的人群中,也有可能存在潛在的癌細胞。梅德澤托夫博士的觀點是,只有當癌細胞與正常細胞形成聯盟時才會生長腫瘤。任何這種關係都有兩面性。
生物入侵是一個級聯方程
一旦我們考慮到疾病是生態系統導致的結果,那麼我們就不得不問為什麼有人不生病。然而,生態學令人沮喪。癌症遺傳學盛行的部分原因是,它解釋了癌症的統一性和多樣性。相比之下,對於生態學家來說,一切都是複雜因素之間的關係。
蒙特婁麥吉爾大學(McGill University)入侵生態學教授安東尼·里卡爾迪博士(Anthony Ricciardi)在聖路易斯河畔長大,這條河正是貽貝前往到北美五大湖的路線。他對我說:「我小時候就在那個湖里玩耍,我熟悉湖里的大部分生物,但從來沒有見過斑馬貽貝。1991年六月的一天,當我正在湖邊研究一個項目時,我翻開一塊石頭,發現附著一個貝殼。我花了幾秒鐘才弄明白它是什麼物種。隨後我又發現了更多貝殼。就是在那時候,我預感到生物入侵」 。
我問他為什麼這些淡水貽貝來到我們的湖泊之後瘋狂生長。他說:「通常把物種引入新環境大多會失敗,往往是因為它們在錯誤的時間到達錯誤的地方,造成大量物種的死亡。水虎魚(piranha)被傾倒在湖里多年,但是它們不能繁殖,因為溫度不合適。人們也曾釋放像比目魚這樣的海洋物種,但鹽度對它們來說不合適。入侵生態學是一種動態,是許多次擲骰子的結果。有很多因素,比如水溫、鹽度、鈣含量、捕食者……儘管其中一些因素明顯比其他因素更重要。單不是單個因素,是一系列因素決定了貽貝怎麼樣和為什麼占據了主導地位」。
生態學家談論營養、捕食者、氣候、地形等因素,構成了複雜的反饋環路,所有因素互為因果。對生態學家來說,物種入侵是一個方程,甚至是一組聯立方程。
對於像我這樣的癌症遺傳學家來說,這是一個沮喪的結論。同樣,考慮到我們的知識,方法和資源的侷限性,癌症領域可能別無選擇,只能屈服於手術刀的傷害,至少目前是這樣。因此大多數癌症生物學家面對生物體的複雜性時,還是將注意力專注於「病原體」:癌細胞。因為研究轉移比研究不轉移性更直接;從臨床上講,很難研究那些沒有生病的人。我們的醫生已經習慣於疾病和健康的區別:活檢是陽性的,血液檢查為陰性,掃瞄發現「沒有疾病的證據」。好的細菌,不好的細菌……
然而,在今年六月的ASCO會議上,我欣喜地發現關於「種子」的研究逐漸為「土壤」研究提供了空間,這種變化帶給我的興奮甚至超過免疫治療的進步。深入研究生態模式會使我們遇到新的問題,但隨著時間的推移,它也可能會讓我們真正的理解癌症。
認真對待分母問題,會帶給我們分母解決方案。在腫瘤學領域,「整體論」已經成為未經驗證的民間偏方的代名詞:覆盆子茶和果汁。然而,隨著雄心勃勃的癌症研究人員開始研究土壤和種子,人們看到了一種新方法論的開始。它將使我們回到「整體」的真正含義:把身體,有機體,解剖結構,生理學這一令人難以置信的錯綜複雜的網絡作為一個整體。這樣的做法會有所幫助我們理解所有令人困擾的多樣性的現象;有助於我們理解什麼時候身體控制了癌症,什麼時候癌症控制了身體。它會鼓勵醫生不僅關心你的病是什麼,而且關心你是誰。
來源:kknews癌症入侵的方程式:癌和患癌的器官,就像種子和土壤